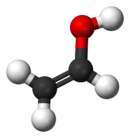
Vinil alkohol
Vinil alkohol, disebut pula sebagai etenol (nama IUPAC), adalah enol paling sederhana. Dengan rumus CH2CHOH, senyawa ini adalah senyawa labil yang mampu berubah menjadi asetaldehida. Senyawa ini bukan merupakan prekursor pada pembentukan polivinil alkohol.
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC (preferensi)
Etenol | |||
| Nama lain
Hidroksietena
Hidroksietilena | |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C2H4O | |||
| Massa molar | 44.053 g/mol | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Tautomerisasi asetaldehida menjadi vinil alkohol
Dalam kondisi normal, vinil alkohol berubah (tautomerisasi) menjadi asetaldehida:
Pada suhu ruangan, asetaldehida (H3CC(O)H) lebih stabil daripada vinil alkohol (H2C=CHOH) dengan 42.7 kJ/mol:[1]
- H2C=CHOH → H3CC(O)H ΔH298,g = −42.7 kJ/mol
Tautomerisasi keto-enol yang tidak dikatalisis melalui migrasi 1,3-hidrogen terlarang oleh Aturan Woodward–Hoffmann dan karena itu memiliki hambatan aktivasi yang tinggi dan bukan jalur yang signifikan pada atau dekat suhu kamar. Namun, bahkan asam atau basa (termasuk air) dengan jumlah penjejak dapat mengkatalisasi reaksi tersebut. Bahkan dengan tindakan pencegahan ketat untuk meminimalkan sumber adventif atau sumber proton, vinil alkohol hanya dapat disimpan selama beberapa menit hingga beberapa jam sebelum diisomerisasi menjadi asetaldehida. (asam karbonat adalah contoh lain dari zat yang stabil secara kinetik ketika murni, tetapi terurai dengan cepat karena katalisis oleh jejak uap air.)
Tautomerisasi juga dapat dikatalisasi melalui proses fotokimia. Temuan ini menunjukkan bahwa tautomerisasi keto-enol adalah rute yang layak di bawah kondisi atmosfer dan stratosfer, yang relevan dengan peran vinil alkohol dalam produksi asam organik di atmosfer.[2][3]
Senyawa ini dapat dibentuk oleh eliminasi pirolitik air dari etilena glikol pada suhu 900 °C dan tekanan yang rendah.[4]
Hubungan dengan poli(vinil alkohol)
Karena ketidakstabilan vinil alkohol, polivinil alkohol termoplastik (PVA atau PVOH) dibuat secara tidak langsung dengan polimerisasi vinil asetat diikuti oleh hidrolisis ikatan ester (Ac = asetil, HOAc = asam asetat):
- n CH2=CHOAc → (CH2−CHOAc)n
- (CH2−CHOAc)n + n H2O → (CH2−CHOH)n + n HOAc
Sebagai ligan
Beberapa kompleks logam diketahui mengandung vinil alkohol sebagai ligan. Salah satu contohnya adalah Pt(acac)(η2-C2H3OH)Cl.[5]
Keberadaan dalam medium antarbintang
Vinil alkohol dideteksi dalam molekul Sagittarius B.[7] Stabilitasnya dalam medium antarbintang (terlarut) menunjukkan bahwa tautomerisasinya tidak unimolekuler.
Lihat pula
Referensi
- ^ R.D. Johnson III. "CCCBDB NIST Standard Reference Database" (dalam bahasa Inggris). Diakses tanggal 30 Agustus 2014.
- ^ Heazlewood, B. R.; Maccarone, A. T.; Andrews, D. U.; Osborn, D. L.; Harding, L. B.; Klippenstein, S. J.; Jordan, M. J. T.; Kable, S. H. "Near-threshold H/D exchange in CD3CHO photodissociation." Nat. Chem. 2011, 3, 443−448. doi:10.1038/nchem.1052
- ^ Andrews, D. U.; Heazlewood, B. R.; Maccarone, A. T.; Conroy, T.; Payne, R. J.; Jordan, M. J. T.; Kable, S. H. "Photo-tautomerization of acetaldehyde to vinyl alcohol: A potential route to tropospheric acids." Science 2012, 337, 1203−1206. doi:10.1126/science.1220712
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart. Organic Chemistry, edisi ke-2, hlm. 456-57. Oxford University Press, 2012. ISBN 978-0-19-927029-3.
- ^ F. A. Cotton, J. N. Francis, B. A. Frenz, M. Tsutsui "Structure of a dihapto(vinyl alcohol) complex of platinum(II)" Journal of the American Chemical Society, 1973, volume 95, p. 2483-6. doi:10.1021/ja00789a011
- ^ J. A. Keith, P. M. Henry (2009). "The Mechanism of the Wacker Reaction: A Tale of Two Hydroxypalladations". Angew. Chem. Int. Ed. 48: 9038–9049. doi:10.1002/anie.200902194.
- ^ "Scientists Toast the Discovery of Vinyl Alcohol in Interstellar Space" (dalam bahasa Inggris). National Radio Astronomy Observatory. 1 Oktober 2001. Diakses tanggal 20 Desember 2006.