Fenoterol
Fenoterol adalah agonis adrenoreseptor β. Obat ini tergolong agonis β2 simpatomimetik dan obat asma bronkodilator hirup.

| |
|---|---|
| |
| Nama sistematis (IUPAC) | |
| (RR,SS)-5-(1-hidroksi-2-{[2-(4-hidroksifenil)-1-metiletil]amino}etil)benzena-1,3-diol | |
| Data klinis | |
| AHFS/Drugs.com | Micromedex Detailed Consumer Information |
| Kat. kehamilan | A(AU) B(US) |
| Status hukum | Harus dengan resep dokter (S4) (AU) |
| Rute | Inhalasi (Inhaler dosis terukur) |
| Data farmakokinetik | |
| Waktu paruh | Sekitar 6,5 jam[1][2][3][4] |
| Pengenal | |
| Nomor CAS | 13392-18-2 |
| Kode ATC | R03AC04 G02CA03 |
| PubChem | CID 3343 |
| Ligan IUPHAR | 557 |
| DrugBank | DB01288 |
| ChemSpider | 3226 |
| UNII | 22M9P70OQ9 |
| KEGG | D04157 |
| ChEBI | CHEBI:149226 |
| ChEMBL | CHEMBL32800 |
| Data kimia | |
| Rumus | C17H21NO4 |
| SMILES | eMolecules & PubChem |
| |
Fenoterol diproduksi dan dijual oleh Boehringer Ingelheim sebagai Berotec N dan dalam kombinasi dengan ipratropium bromida sebagai Berodual N.
Obat ini dipatenkan pada tahun 1962 dan mulai digunakan dalam dunia medis pada tahun 1971[5], tetapi pada tahun 1980-an, muncul kekhawatiran tentang keamanannya dan penggunaannya yang dikaitkan dengan peningkatan risiko kematian (lihat di bawah).
Efek samping dan toksisitas
suntingFenoterol adalah agonis β2 kerja pendek yang juga menstimulasi reseptor β1. Fenoterol memiliki toksisitas kardiovaskular yang lebih besar daripada isoprenalin atau salbutamol.[6][7] Fenoterol digunakan secara luas di Selandia Baru pada akhir tahun 1970-an dan 1980-an hingga dihapus dari tarif obat Selandia Baru pada tahun 1989 karena pengenalan dan penggunaan luasnya dikaitkan dengan epidemi kematian akibat asma.[8] Serangkaian studi kasus-kontrol menunjukkan bahwa penderita asma yang menggunakan fenoterol lebih mungkin meninggal karena asma dibandingkan dengan kontrol yang diobati dengan agonis beta alternatif; risiko kematian asma ini sangat tinggi pada penderita asma parah.[9][10] Angka kematian menurun setelah penghentian fenoterol[11] tanpa bukti yang mendukung penjelasan alternatif untuk kenaikan dan penurunan mendadak kematian akibat asma.[12] Data tidak mendukung efek pengacau berdasarkan tingkat keparahan sebagai penjelasan untuk kelebihan kematian.[13] Ada agonis beta kerja pendek alternatif yang tidak dikaitkan dengan peningkatan mortalitas, misalnya salbutamol.
Stereoisomer
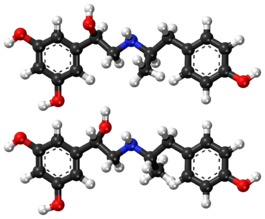
sunting5-(1-Hidroksi-2-{[2-(4-hidroksifenil)-1-metiletil]amino}etil)benzena-1,3-diol adalah molekul dengan dua pusat stereogenik yang berbeda. Dengan demikian, empat stereoisomer mungkin ada, yaitu stereoisomer (R,R)-, (R,S)-, (S,R)- dan (S,S)- (lihat gambar di bawah). Fenoterol adalah rasemat dari enantiomer (R,R)- dan (S,S). Rasemat ini 9 hingga 20 kali lebih efektif, dibandingkan dengan rasemat dari enantiomer (R,S)- dan (S,R).[14]
Referensi
sunting- ^ "Fenoterol Hydrobromide Drug Information, Professional". Drugs.com. 1996-01-01. Diarsipkan dari versi asli tanggal 2019-08-25. Diakses tanggal 2018-06-11.
- ^ "Fenoterol - Drug Monograph". DrugInfoSys.com. 2016-10-27. Diakses tanggal 2018-06-11.
- ^ "Berotec Inhalation Solution (Fenoterol HBr)". RxMed.com. Diakses tanggal 2018-06-11.
- ^ Svedmyr N (1985-05-06). "Fenoterol: A Beta2-adrenergic Agonist for Use in Asthma; Pharmacology, Pharmacokinetics, Clinical Efficacy and Adverse Effects". Pharmacotherapy. Wiley. 5 (3): 109–126. doi:10.1002/j.1875-9114.1985.tb03409.x. ISSN 0277-0008. PMID 2991865.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. hlm. 542. ISBN 9783527607495.
- ^ Crane J, Burgess C, Beasley R (February 1989). "Cardiovascular and hypokalaemic effects of inhaled salbutamol, fenoterol, and isoprenaline". Thorax. 44 (2): 136–40. doi:10.1136/thx.44.2.136. PMC 461717 . PMID 2928998.
- ^ Burgess CD, Windom HH, Pearce N, Marshall S, Beasley R, Siebers RW, Crane J (February 1991). "Lack of evidence for beta-2 receptor selectivity: a study of metaproterenol, fenoterol, isoproterenol, and epinephrine in patients with asthma". The American Review of Respiratory Disease. 143 (2): 444–6. doi:10.1164/ajrccm/143.2.444. PMID 1671326.
- ^ Beasley R, Pearce N, Crane J, Burgess C (1995). "Withdrawal of fenoterol and the end of the New Zealand asthma mortality epidemic". International Archives of Allergy and Immunology. 107 (1–3): 325–7. doi:10.1159/000237016. PMID 7613161.
- ^ Crane J, Pearce N, Flatt A, Burgess C, Jackson R, Kwong T, Ball M, Beasley R (April 1989). "Prescribed fenoterol and death from asthma in New Zealand, 1981-83: case-control study". Lancet. 1 (8644): 917–22. doi:10.1016/s0140-6736(89)92505-1. PMID 2565417.
- ^ Pearce N, Grainger J, Atkinson M, Crane J, Burgess C, Culling C, Windom H, Beasley R (March 1990). "Case-control study of prescribed fenoterol and death from asthma in New Zealand, 1977-81". Thorax. 45 (3): 170–5. doi:10.1136/thx.45.3.170. PMC 462377 . PMID 2330548.
- ^ Beasley R, Pearce N, Crane J, Burgess C (1995). "Withdrawal of fenoterol and the end of the New Zealand asthma mortality epidemic". International Archives of Allergy and Immunology. 107 (1–3): 325–7. doi:10.1159/000237016. PMID 7613161.
- ^ Pearce N, Beasley R, Crane J, Burgess C, Jackson R (January 1995). "End of the New Zealand asthma mortality epidemic". Lancet (dalam bahasa English). 345 (8941): 41–4. doi:10.1016/s0140-6736(95)91159-6. PMID 7799709.
- ^ Beasley R, Burgess C, Pearce N, Woodman K, Crane J (July 1994). "Confounding by severity does not explain the association between fenoterol and asthma death". Clinical and Experimental Allergy. 24 (7): 660–8. doi:10.1111/j.1365-2222.1994.tb00970.x. PMID 7953948.
- ^ Beale JP, Stephenson NC (April 1972). "X-ray analysis of Th 1165a* and salbutamol". Journal of Pharmacy and Pharmacology. 24 (4): 277–280. doi:10.1111/j.2042-7158.1972.tb08986.x. PMID 4402834.