Air raja
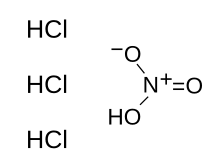
Aqua regia (bahasa Latin yang berarti "air raja") adalah larutan yang dibuat dari percampuran asam klorida pekat (HCl) dan asam nitrat pekat (HNO) dengan perbandingan 3:1.[1] Larutan ini bersifat sangat korosif mengeluarkan uap berwarna kuning. Hanya larutan inilah yang sanggup melarutkan raksa, timbal, emas dan platina (logam-logam yang paling mulia menurut deret Volta), oleh karena itulah disebut sebagai aqua regia atau Air Raja. Karena sifatnya yang kurang stabil, maka larutan ini baru dibuat jika akan dipakai.
| |
| Nama | |
|---|---|
| Nama IUPAC
nitric acid hydrochloride
| |
| Nama lain
aqua regis, nitrohydrochloric acid
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| Sifat | |
| HNO3 + 3HCl | |
| Penampilan | cairan berasap berwarna merah, kuning atau emas |
| Densitas | 1,01–1,21 g/cm3 |
| Titik lebur | −42 C |
| Titik didih | 108 C |
| dapat campur dengan air | |
| Tekanan uap | 21 mbar |
| Bahaya | |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |


Aplikasi
Kegunaan utama aqua regia adalah untuk membuat asam kloroaurat, elektrolit dalam proses Wohlwill untuk pengolahan emas berkualitas tinggi (99.999%).
Aqua regia juga digunakan dalam etsa dan dalam prosedur analisis kimia. Air raja juga digunakan dalam laboratorium untuk mencuci peralatan gelas untuk senyawa organik dan partikel logam. Metode ini lebih disukai dibandingkan penangas asam kromat untuk mencuci tabung NMR, karena tidak ada residu krom yang bersifat paramagnetik yang dapat mengganggu spektrum.[2] Sementara penangas asam kromat kurang disukai karena toksisitas kromium yang tinggi dan berpotensi ledakan, aqua regia sangat korosif dan bertanggung jawab pada beberapa ledakan akibat salah penanganan.[3]
Oleh karena reaksi antar komponennya menyebabkan dekomposisi, aqua regia cepat kehilangan efektivitasnya (meski tetap asam kuat), sehingga komponen-komponennya biasanya dicampur segera sebelum digunakan.
Meskipun peraturan lokal bervariasi, aqua regia dapat dinetralisasi dengan hati-hati sebelum dibuang ke saluran pembuangan. Jika ada kontaminasi oleh logam terlarut, larutan hasil netralisasi harus dikumpulkan untuk dibuang.[4][5]
Kimia
Melarutkan emas
Aqua regia melarutkan emas, meski asam penyusunnya tidak dapat melakukannya jika berdiri sendiri, karena, dalam kombinasi, masing-masing asam melakukan tugas yang berbeda. Asam nitrat adalah oksidator kuat, yang melarutkan sejumlah emas yang hampir tidak terdeteksi, membentuk ion emas (Au). Asam klorida menyediakan pasokan ion klorida (Cl), yang bereaksi dengan ion emas menghasilkan anion tetrakloroaurat(III), juga dalam larutan. Reaksi dengan asam hidroklorida adalah reaksi kesetimbangan yang disertai pembentukan anion kloroaurat (AuCl). Hal ini menyebabkan pengangkatan ion emas dari larutannya dan memungkinkan terjadinya oksidasi emas lebih lanjut. Emas larut menjadi asam kloroaurat. Selain itu, emas dapat dilarutkan oleh klor bebas yang terdapat dalam aqua regia. Persamaan yang sesuai adalah:
- Au + 3 HNO + 4 HCl [AuCl''"; + 3 [NO''"; + [H''"; + 2 H
- atau
- Au + HNO + 4 HCl [AuCl''"; + [NO] + [H''"; + H
Jika larutan aqua regia hanya mengandung emas, asam tetrakloroaurat padat dapat dibuat dengan merebus kelebihan aqua regia, dan menghilangkan sisa asam nitrat dengan pemanasan berulang-ulang menggunakan asam klorida. Langkah tersebut mereduksi asam nitrat (lihat dekomposisi aqua regia). Jika diinginkan emas elemental, ia dapat direduksi secara selektif menggunakan belerang dioksida, hidrazin, asam oksalat, dll.[6] Persamaan yang sesuai adalah, sebagai contoh:
- 2AuCl(aq) + 3SO(g) + 6H(l) → 2Au(s) + 12H(aq) + 3SO(aq) + 8Cl(aq)
Melarutkan platina
Persamaan serupa dapat ditulis untuk platina. Seperti emas, reaksi oksidasi dapat ditulis dengan nitrogen oksida atau nitrogen dioksida sebagai produk oksida nitrogen.
- Pt(s) + 4NO(aq) + 8H+(aq) → Pt(aq) + 4NO(g) + 4H(l)
- 3Pt(s) + 4NO(aq) + 16H(aq) → 3Pt(aq) + 4NO(g) + 8H(l)
Ion platina yang teroksidasi kemudian bereaksi dengan ion klorida menghasilkan ion kloroplatinat.
- Pt(aq) + 6Cl−(aq) → PtCl(aq)
Bukti eksperimental menunjukkan bahwa reaksi platina dengan aqua regia jauh lebih kompleks. Reaksi awal menghasilkan campuran asam kloroplatina(II) (H) dan nitrosoplatinat klorida ((NO)). Nitrosoplatinat klorida berupa padatan. Jika diinginkan pelarutan platina secara total, harus dilakukan ekstraksi padatan residu secara berulang dengan asam klorida pekat.
- 2Pt(s) + 2HNO(aq) + 8HCl(aq) → (NO)(s) + H(aq) + 4H(l)
- (NO)(s) + 2HCl(aq) H(aq) + 2NOCl(g)
Asam kloroplatina(II) dapat dioksidasi menjadi asam kloroplatinat dengan cara menjenuhkan larutan dengan klorin saat pemanasan.
- H(aq) + Cl(g) → H(aq)
Melarutkan platina dalam aqua regia adalah cara untuk mendapatkan logam yang paling padat, iridium dan osmium, keduanya ditemukan dalam bijih platina dan tidak dapat larut dalam asam, sehingga mengendap di dasar bejana.
Secara praktis, ketika logam golongan platina dimurnikan melalui pelarutan dalam aqua regia, emas (umumnya dikaitkan dengan PGM) diendapkan melalui perlakuan dengan besi(II) klorida. Platina dalam filtrat, seperti heksakloroplatinat(VI), diubah menjadi amonium heksakloroplatinat dengan penambahan amonium klorida. Garam amonium ini sangat tidak larut, dan bisa disaring. Pengapian (pemanasan kuat) mengubahnya menjadi logam platina:[7]
- 3(NH''"; → 3Pt + 2N + 2NH + 16HCl
Heksakloroplatinat(IV) yang tak mengendap direduksi dengan unsur zinc, dan metode serupa cocok untuk pemulihan platina dalam skala kecil dari residu laboratorium.[8]
-
Sekeping koin komemoratif platina Uni Soviet dilarutkan dalam aqua regia.
Reaksi dengan timah
Aqua regia bereaksi dengan timah membentuk timah(IV) klorida, yang mengandung timah dalam tingkat oksidasi tertingginya:
- 4HCl + 2HNO + Sn → SnCl + NO + NO + 3H
Dekomposisi aqua regia
Reaksi kimia terjadi saat pencampuran asam klorida pekat dan asam nitrat pekat. Reaksi ini menghasilkan produk volatil nitrosil klorida dan klor yang dibuktikan dengan sifat dan karakteristik asap kuning aqua regia. Oleh karena produk volatil keluar dari larutan, aqua regia kehilangan potensinya.
- HNO(aq) + 3HCl(aq) → NOCl(g) + Cl(g) + 2H(l)
Nitrosil klorida dapat terurai lebih lanjut menjadi nitrogen monoksida dan klor. Disosiasi ini adalah kesetimbangan terbatas. Oleh karena itu, selain nitrosil klorida dan klorin, asap di atas aqua regia mengandung nitrogen monoksida.
- 2NOCl(g) → 2NO(g) + Cl2(g)
Oleh karena nitrogen monoksida mudah bereaksi dengan oksigen atmosfer, gas yang dihasilkan juga mengandung nitrogen dioksida, NO.
- 2NO(g) + O(g) → 2NO(g)
Sejarah
Lihat juga
Catatan
- ^ Informasi dalam infobox ini akurat jika dan hanya jika rasio molar asam nitrat terhadap asam klorida adalah 1:3.
Referensi
- ^ Konsentrasi relatif kedua asam dalam air berbeda, nilainya berkisar 65% b/v untuk asam nitrat dan 35% b/v untuk asam klorida — artinya, perbandingan massa aktual HNO:HCl adalah kurang dari 1:2
- ^ Hoffman, R. (10 March 2005) How to make an NMR sample, Hebrew University. Diakses 31 Oktober 2006.
- ^ American Industrial Hygiene Association, Laboratory Safety Incidents: Explosions. Diakses 8 September 2010.
- ^ Committee on Prudent Practices for Handling, Storage, and Disposal of Chemicals in Laboratories, National Research Council (1995). Prudent Practices in the Laboratory: Handling and Disposal of Chemicals (free fulltext). National Academies Press. hlm. 160–161.
- ^ "Aqua Regia". Laboratory Safety Manual. Princeton University.
- ^ Renner, Hermann; Schlamp, Günther; Hollmann, Dieter; Lüschow, Hans Martin; Tews, Peter; Rothaut, Josef; Dermann, Klaus; Knödler, Alfons; et al. (2005), "Gold, Gold Alloys, and Gold Compounds", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a12_499
- ^ Hunt, L. B.; Lever, F. M. (1969). "Platinum Metals: A Survey of Productive Resources to industrial Uses" (PDF). Platinum Metals Review. 13 (4): 126–138.
- ^ Kauffman, George B.; Teter, Larry A.; Rhoda, Richard N. (1963). "Recovery of Platinum from Laboratory Residues". Inorg. Synth. Inorganic Syntheses. 7: 232. doi:10.1002/9780470132388.ch61. ISBN 9780470132388.