Spektroskopi Raman
Spektroskopi Raman (/ˈrɑːmən/; dinamai dari Sir C. V. Raman) adalah sebuah teknik spektroskopi yang digunakan untuk mengamati mode vibrasional, rotasional, dan mode frekuensi-rendah lainnya dalam suatu sistem.[1] Spektroskopi Raman umum digunakan dalam ilmu kimia untuk menyediakan sidik jari yang dengannya molekul dapat diidentifikasi.
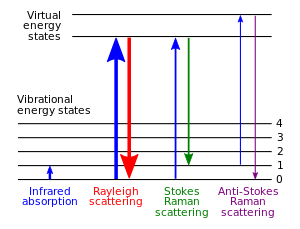
Teknik ini bergantung pada hamburan inelastik, atau hamburan Raman, pada cahaya monokrom, biasanya dari suatu laser dalam rentang kasatmata, dekat inframerah, atau dekat ultraviolet. Cahaya laser berinteraksi dengan vibrasi molekul, fonon atau eksitasi lainnya dalam sistem, menghasilkan energi pada foton laser mengalami pergeseran naik atau turun. Pergeseran energi memberikan informasi tentang mode vibrasional dalam sistem. Spektroskopi inframerah memberi hasil yang serupa, tetapi mendukung, informasi tersebut.
Prinsip
Secara khusus, sampel diiluminasi dengan tembakan laser. Radiasi elektromagnetik dari lokasi yang diiluminasi dikumpulkan dengan suatu lensa dan dikirim melalui suatu monokromator. Radiasi hamburan elastis pada panjang gelombang yang sesuai dengan garis laser (hamburan Rayleigh) dipisahkan baik menggunakan notch filter, edge pass filter, atau band pass filter, sementara sisa cahaya yang terkumpul didispersikan pada suatu detektor.
Hamburan Raman spontan secara khusus sangat lemah, dan sebagai hasilnya kesulitan utama pada spektroskopi Raman adalah memisahkan hamburan cahaya tidak elastis yang lemah dari hamburan Rayleigh pada cahaya laser yang intens. Dalam sejarah, spektrometer Raman menggunakan grating hologram dan dispersi multi-tahap untuk mendapat rejeksi laser dengan derajat yang tinggi. Di masa lampau, fotomultiplier merupakan detektor pilihan untuk pengaturan dispersif Raman, yang menghasilkan waktu perolehan panjang. Namun, instrumentasi modern yang hampir secara universal mempekerjakan notch atau edge filters untuk rejeksi laser dan spektrograf baik berupa transmisif aksial (AT), Monokromator Czerny–Turner (CT), atau FT (berbasis spektroskopi transformasi Fourier), dan detektor CCD.
Pergeseran Raman
Pergeseran Raman secara khusus dilaporkan dalam bilangan gelombang, yang memiliki satuan berbanding-terbalik panjangnya, karena nilai tersebut berhubungan langsung dengan energi. Untuk mengkonversi panjang gelombang spektrum dan bilangan gelombang pada pergeseran dalam spektrum Raman, rumus berikut dapat digunakan:
di mana adalah pergeseran Raman yang dinyatakan dalam bilangan gelombang, λ0 adalah panjang gelombang eksitasi, dan λ1 adalah panjang gelombang spektrum Raman. Secara umum, satuan untuk menyatakan bilangan gelombang dalam spektrum Raman adalah kebalikan dari sentimeter (cm−1). Karena panjnag gelombang terkadang dinyatakan dalam satuan nanometer (nm), rumus di atas dapat diskalakan dalam konversi satuan tersebut secara eksplisit, menghasilkan
Aplikasi
Spektroskopi Raman umum digunakan dalam ilmu kimia, karena informasi vibrasional spesifik untuk ikatan kimia dan simetri molekul. Karenanya, ia memberikan sidik jari di mana molekul dapat diidentifikasi. Misalnya, frekuensi vibrasional untuk SiO, Si2O2, dan Si3O3 diidentifikasi dan ditetapkan atas dasar koordinat analisis yang normal menggunakan spektrum inframerah dan Raman.[2] Daerah sidik jari bagi molekul organik adalah pada rentang (bilangan gelombang) 500–2000 cm−1. Cara lainnya bahwa teknik ini digunakan adalah untuk mempelajari perubahan ikatan kimia, seperti ketika substrat ditambahkan pada enzim.
Beberapa proyek penelitian menunjukkan penggunaan spektroskopi Raman sebagai sarana untuk mendeteksi peledak menggunakan sinar laser dari jarak yang aman (Portendo, 2008,[3] TU Vienna, 2012[4]).[5]
Spektroskopi Raman juga telah digunakan untuk mengkonfirmasi prediksi keberadaan fonon berfrekuensi rendah[6] dalam protein dan DNA,[7][8][9][10] menstimulasi studi bagi pergerakan kolektif berfrekuensi rendah dalam protein dan DNA dan fungsi biologis mereka.[11][12]
Raman melaporkan molekul dengan gugus olefin atau alkuna tengah dikembangkan untuk memungkinkan untuk pencitraan jaringan dengan antibodi berlabel-SERS[13] Spektroskopi Raman juga telah digunakan sebagai teknik noninvasif secara aktual, karakterisasi biokimia in situ pada penyembuhan luka serta analisis multivariat spektrum Raman telah memungkinkan pengukuran kuantitatif dari kemajuan penyembuhan luka.[14] Spektroskopi Raman memiliki penggunaan luas dalam studi biomineral.[15]
Lihat pula
Referensi
- ^ Gardiner, D.J. (1989). Practical Raman spectroscopy. Springer-Verlag. ISBN 978-0-387-50254-0.
- ^ Khanna, R.K. (1981). "Raman-spectroscopy of oligomeric SiO species isolated in solid methane". Journal of Chemical Physics. 74 (4): 2108. Bibcode:1981JChPh..74.2108K. doi:10.1063/1.441393.
- ^ Ben Vogel (29 August 2008). "Raman spectroscopy portends well for standoff explosives detection". Jane's. Diarsipkan dari versi asli tanggal 2008-12-03. Diakses tanggal 2008-08-29.
- ^ "Finding explosives with laser beams", rilis pers TU Vienna
- ^ Misra, Anupam K.; Sharma, Shiv K.; Acosta, Tayro E.; Porter, John N.; et al. (2012). "Single-Pulse Standoff Raman Detection of Chemicals from 120 m Distance During Daytime". Applied Spectroscopy. 66 (11): 1279–85. doi:10.1366/12-06617. PMID 23146183.
- ^ Chou, Kuo-Chen; Chen, Nian-Yi (1977). "The biological functions of low-frequency phonons". Scientia Sinica. 20 (3): 447–457.
- ^ Urabe, H.; Tominaga, Y.; Kubota, K. (1983). "Experimental evidence of collective vibrations in DNA double helix Raman spectroscopy". Journal of Chemical Physics. 78 (10): 5937–5939. Bibcode:1983JChPh..78.5937U. doi:10.1063/1.444600.
- ^ Chou, K.C. (1983). "Identification of low-frequency modes in protein molecules". Biochemical Journal. 215 (3): 465–469. doi:10.1042/bj2150465. PMC 1152424 . PMID 6362659.
- ^ Chou, K.C. (1984). "Low-frequency vibration of DNA molecules". Biochemical Journal. 221 (1): 27–31. doi:10.1042/bj2210027. PMC 1143999 . PMID 6466317.
- ^ Urabe, H.; Sugawara, Y.; Ataka, M.; Rupprecht, A. (1998). "Low-frequency Raman spectra of lysozyme crystals and oriented DNA films: dynamics of crystal water". Biophys J. 74 (3): 1533–1540. doi:10.1016/s0006-3495(98)77865-8. PMC 1299499 . PMID 9512049.
- ^ Chou, Kuo-Chen (1988). "Review: Low-frequency collective motion in biomacromolecules and its biological functions". Biophysical Chemistry. 30 (1): 3–48. doi:10.1016/0301-4622(88)85002-6. PMID 3046672.
- ^ Chou, K.C. (1989). "Low-frequency resonance and cooperativity of hemoglobin". Trends in Biochemical Sciences. 14 (6): 212–3. doi:10.1016/0968-0004(89)90026-1. PMID 2763333.
- ^ Schlücker, S.; et al. (2011). "Design and synthesis of Raman reporter molecules for tissue imaging by immuno-SERS microscopy". Journal of Biophotonics. 4 (6): 453–463. doi:10.1002/jbio.201000116. PMID 21298811.
- ^ Jain, R.; et al. (2014). "Raman Spectroscopy Enables Noninvasive Biochemical Characterization and Identification of the Stage of Healing of a Wound". Analytical Chemistry. 86 (8): 3764–3772. doi:10.1021/ac500513t. PMC 4004186 . PMID 24559115.
- ^ Taylor, P.D.; Vinn, O.; Kudryavtsev, A.; Schopf, J.W. (2010). "Raman spectroscopic study of the mineral composition of cirratulid tubes (Annelida, Polychaeta)". Journal of Structural Biology. 171 (3): 402–405. doi:10.1016/j.jsb.2010.05.010. PMID 20566380. Diakses tanggal 10 Juni 2014.
Pranala luar
- DoITPoMS Teaching and Learning Package – Raman Spectroscopy – pengantar spektroskopi Raman, ditujukan untuk tingkat sarjana.
- Spektroskopi Raman dalam analisis lukisan, ColourLex