Virus
Virus adalah mikroorganisme patogen yang hanya dapat bereplikasi di dalam sel makhluk hidup karena mereka tidak memiliki perlengkapan seluler untuk bereproduksi sendiri. Semua bentuk kehidupan dapat diinfeksi oleh virus, mulai dari hewan, tumbuhan, hingga bakteri dan arkea.[2] Istilah virus biasanya digunakan untuk menyebut jenis virus yang menginfeksi sel-sel eukariota, sementara virus yang menginfeksi sel prokariota (seperti bakteri dan arkea) dikenal sebagai bakteriofag. Keberadaan virus pertama kali diketahui melalui tulisan ilmiah Dmitri Ivanovsky pada 1892 yang menguraikan patogen non-bakteri yang menginfeksi tanaman tembakau dan penemuan virus mosaik tembakau oleh Martinus Beijerinck pada tahun 1898.[3] Hingga tahun 2019, lebih dari 6.000 spesies virus telah dideskripsikan secara rinci,[1] dari total jutaan jenis virus di lingkungan.[4] Virus ditemukan di hampir setiap ekosistem di Bumi dan merupakan entitas biologis yang paling banyak jumlahnya.[5][6] Ilmu yang mempelajari tentang virus dikenal sebagai virologi, sebuah subspesialisasi mikrobiologi.
| Virus | |
|---|---|
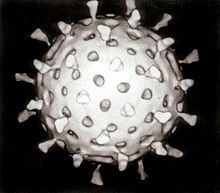
| |
| Rekonstruksi partikel Rotavirus menggunakan komputer. | |
| Klasifikasi virus | |
| Dunia[1] | |
Saat terinfeksi, sel inang dipaksa untuk menghasilkan ribuan salinan identik dari virus asli dengan cepat. Ketika tidak berada di dalam sel atau tidak dalam proses menginfeksi sel, virus berada dalam bentuk partikel independen yang disebut virion. Virion terdiri atas dua atau tiga bagian: (1) materi genetik, yaitu molekul panjang asam nukleat (berupa DNA saja atau RNA saja, tetapi tidak kombinasi keduanya) yang menyandi struktur protein yang digunakan virus; (2) mantel protein yang disebut kapsid, berfungsi mengelilingi dan melindungi materi genetik; dan pada sebagian virus terdapat (3) selubung atau amplop luar yang terbuat dari lipid. Bentuk partikel virus berkisar dari bentuk heliks (pilinan) sederhana, ikosahedral (bangun ruang bersisi 20), hingga struktur yang lebih kompleks. Kebanyakan spesies virus memiliki virion yang terlalu kecil untuk dilihat dengan mikroskop cahaya karena ukurannya seperseratus dari bakteri pada umumnya.
Asal-usul virus dalam sejarah evolusi kehidupan masih belum jelas: beberapa virus mungkin berevolusi dari plasmid (potongan DNA yang dapat berpindah antarsel), sementara yang lain mungkin berevolusi dari bakteri. Dalam evolusi, virus merupakan perantara penting dalam transfer gen horizontal, yang meningkatkan keanekaragaman genetik dengan cara yang dianalogikan dengan reproduksi seksual.[7] Ada perbedaan pendapat ilmiah mengenai status virus sebagai makhluk hidup atau sebagai struktur organik yang berinteraksi dengan makhluk hidup.[8] Sebagai bentuk kehidupan, virus membawa materi genetik, berkembang biak, dan berevolusi melalui seleksi alam, meskipun mereka tidak memiliki karakteristik utama makhluk hidup, seperti struktur sel, yang umumnya dianggap sebagai kriteria yang diperlukan untuk kehidupan. Karena mereka memiliki beberapa kriteria makhluk hidup tetapi tidak semuanya, virus digambarkan sebagai "organisme di tepi kehidupan",[9] dan sebagai pengganda diri.[8]
Virus menyebar dengan berbagai cara. Salah satu jalur penularan adalah melalui organisme pembawa penyakit yang dikenal sebagai vektor: misalnya, virus sering ditularkan dari tumbuhan satu ke tumbuhan oleh serangga yang memakan getah tumbuhan, seperti kutu daun; dan virus pada hewan dapat dibawa oleh serangga pengisap darah. Virus influenza menyebar melalui batuk dan bersin. Norovirus dan Rotavirus, penyebab umum gastroenteritis viral, ditularkan melalui jalur fekal–oral, melalui kontak dari-tangan-ke-mulut atau terbawa dalam makanan atau air. Dosis infeksius Norovirus yang diperlukan untuk menghasilkan infeksi pada manusia kurang dari 100 partikel.[10] HIV merupakan salah satu dari beberapa virus yang ditularkan melalui hubungan seksual dan terpapar darah yang mengandung virus. Beragam variasi sel inang yang dapat diinfeksi oleh suatu virus disebut "kisaran inang". Kisaran ini bisa saja sempit, artinya virus tersebut hanya mampu menginfeksi beberapa spesies, atau luas, artinya ia mampu menginfeksi banyak spesies.[11]
Infeksi virus pada hewan memicu respons kekebalan yang biasanya menghilangkan virus yang menginfeksi. Respons kekebalan juga dapat dihasilkan oleh vaksin, yang memberikan kekebalan buatan terhadap infeksi virus tertentu. Beberapa virus, termasuk yang menyebabkan AIDS, infeksi papilomavirus manusia, dan virus hepatitis, menghindari respons kekebalan ini dan menyebabkan infeksi kronis. Beberapa obat antivirus telah dikembangkan untuk mengobati penyakit akibat virus.
Etimologi
Kata virus berasal dari bahasa Latin vīrus yang berarti racun dan cairan berbahaya lainnya, yang lebih jauh berasal dari rumpun bahasa Indo-Eropa lain seperti bahasa Sanskerta viṣa, bahasa Avesta vīša, dan bahasa Yunani Kuno ἰός yang semuanya berarti racun.[12] Kata sifat virulen dari bahasa Latin virulentus yang artinya beracun muncul sekitar tahun 1400.[13] Makna virus sebagai "agen yang mengakibatkan penyakit infeksi" pertama kali digunakan pada tahun 1728,[12] jauh sebelum ditemukannya virus itu sendiri oleh Dmitri Ivanovsky pada tahun 1892. Sementara itu, kata sifat viral yang berarti "dari sifat virus atau disebabkan oleh virus" baru muncul pada tahun 1944.[14] Istilah virion yang tercatat sejak 1959 juga digunakan untuk merujuk pada partikel virus tunggal yang keluar dari sel dan mampu menginfeksi sel lainnya yang sejenis.
Sejarah penemuan
- Virus telah menginfeksi sejak zaman sebelum Masehi, hal tersebut terbukti dengan adanya beberapa penemuan-penemuan yaitu laporan mengenai infeksi virus dalam hieroglif di Memphis, ibu kota Mesir kuno (1400 SM) yang menunjukkan adanya penyakit poliomyelitis. Selain itu, Raja Firaun Ramses V meninggal pada 1196 SM dan dipercaya meninggal karena terserang virus smallpox.
- Pada zaman sebelum Masehi, virus endemik yang cukup terkenal adalah virus smallpox yang menyerang masyarakat Tiongkok pada tahun 1000. Akan tetapi pada pada tahun 1798, Edward Jenner menemukan bahwa beberapa pemerah susu memiliki kekebalan terhadap virus pox. Hal tersebut diduga karena virus pox yang terdapat pada sapi, melindungi manusia dari pox. Penemuan tersebut yang dipahami kemudian merupakan pelopor penggunaan vaksin.
- Pada tahun 1880, Louis Pasteur dan Robert Koch mengemukakan suatu "germ theory" yaitu bahwa mikroorganisme merupakan penyebab penyakit. Pada saat itu juga terkenal Postulat Koch yang sangat terkenal hingga saat ini, yaitu:
- Agen penyakit harus ada di dalam setiap kasus penyakit
- Agen harus bisa diisolasi dari inang dan bisa ditumbuhkan secara in vitro
- Ketika kultur agen muri diinokulasikan ke dalam sel inang sehat yang rentan maka dapat menimbulkan penyakit
- Agen yang sama dapat diambil dan diisolasi kembali dari inang yang terinfeksi tersebut
- Penelitian mengenai virus dimulai dengan penelitian mengenai penyakit mosaik yang menghambat pertumbuhan tanaman tembakau dan membuat daun tanaman tersebut memiliki bercak-bercak. Pada tahun 1883, Adolf Mayer, seorang ilmuwan Jerman, menemukan bahwa penyakit tersebut dapat menular ketika tanaman yang ia teliti menjadi sakit setelah disemprot dengan getah tanaman yang sakit. Karena tidak berhasil menemukan mikrob pada getah tanaman tersebut, Mayer menyimpulkan bahwa penyakit tersebut disebabkan oleh bakteri yang lebih kecil dari biasanya dan tidak dapat dilihat dengan mikroskop.
- Pada tahun 1892, Dmitri Ivanovsky dari Rusia menemukan bahwa getah daun tembakau yang sudah disaring dengan penyaring bakteri masih dapat menimbulkan penyakit mosaik. Ivanowsky lalu menyimpulkan dua kemungkinan, yaitu bahwa bakteri penyebab penyakit tersebut berbentuk sangat kecil sehingga masih dapat melewati saringan, atau bakteri tersebut mengeluarkan toksin yang dapat menembus saringan.[15] Kemungkinan kedua ini dibantah pada tahun 1897 setelah Martinus Beijerinck dari Belanda menemukan bahwa agen infeksi di dalam getah yang sudah disaring tersebut dapat bereproduksi karena kemampuannya menimbulkan penyakit tidak berkurang setelah beberapa kali ditransfer antartanaman.[15] Patogen mosaik tembakau disimpulkan sebagai bukan bakteri, melainkan merupakan contagium vivum fluidum, yaitu sejenis cairan hidup pembawa penyakit.[15]
- Setelah itu, pada tahun 1898, Loeffler dan Frosch melaporkan bahwa penyebab penyakit mulut dan kaki sapi dapat melewati saringan yang tidak dapat dilewati bakteri. Namun, mereka menyimpulkan bahwa patogennya adalah bakteri yang sangat kecil.[15]
- Pendapat Beijerinck baru terbukti pada tahun 1935, setelah Wendell Meredith Stanley dari Amerika Serikat berhasil mengkristalkan partikel penyebab penyakit mosaik yang kini dikenal sebagai virus mosaik tembakau.[16] Stanley mengemukakan bahwa vurus tetap akan dapat tetap aktif meskipun setelah kristalisasi.[17] Virus ini juga merupakan virus yang pertama kali divisualisasikan dengan mikroskop elektron pada tahun 1939 oleh ilmuwan Jerman G.A. Kausche, E. Pfankuch, dan H. Ruska.[18]
- Pada tahun 1911, Peyton Rous menemukan jika ayam yang sehat diinduksi dengan sel tumor dari ayam yang sakit, maka pada ayam yang sehat tersebut juga akan terkena kanker.[19] Selain itu, Rous juga mencoba melisis sel tumor dari ayam yang sakit lalu menyaring sari-sarinya dengan pori-pori yang tidak dapat dilalui oleh bakteri, lalu sari-sari tersebut di suntikkan dalam sel ayam yang sehat dan ternyata hal tersebut juga dapat menyebabkan kanker.[19] Rous menyimpulkan kanker disebabkan karena sel virus pada sel tumor ayam yang sakit yang menginfeksi sel ayam yang sehat.[19] Penemuan tersebut merupakan penemuan pertama virus onkogenik, yaitu virus yang dapat menyebabkan tumor. Virus yang ditemukan oleh Rous dinamakan Rous Sarcoma Virus (RSV).[19]
- Pada tahun 1933, Shope papilloma virus atau cottontail rabbit papilloma virus (CRPV) yang ditemukan oleh Dr. Richard E Shope merupakan model kanker pertama pada manusia yang disebabkan oleh virus.[20] Dr. Shope melakukan percobaan dengan mengambil filtrat dari tumor pada hewan lalu disuntikkan pada kelinci domestik yang sehat, dan ternyata timbul tumor pada kelinci tersebut.[20]
- Martha Chase dan Alfred Hershey pada tahun 1952 berhasil menemukan bakteriofag.[21] Bakteriofag merupakan virus yang memiliki inang bakteri sehingga hanya dapat bereplikasi di dalam sel bakteri.[21]
Asal-usul
Virus selalu berdampingan dengan organisme, dan mungkin telah ada sejak sel hidup pertama kali berevolusi. Virus tidak meninggalkan fosil, sehingga asal muasal virus hanya bisa dihipotesiskan dengan cara-cara seperti teknik-teknik biologi molekuler. Teknik-teknik ini mengandalkan keberadaan DNA atau RNA virus yang terdahulu. Akan tetapi, sebagian besar virus yang diawetkan dan disimpan di laboratorium berusia kurang dari 90 tahun.[22][23] Metode-metode biologi molekuler hanya berhasil melacak nenek moyang virus yang berevolusi pada abad ke-20.[24] Golongan virus baru berkali-kali muncul dalam berbagai tahap evolusi makhluk hidup.[25] Ada tiga teori utama tentang asal-usul virus: teori regresi, teori keluar dari sel, dan teori koevolusi[25][26]
- Teori regresi
- Menurut teori ini, virus bisa jadi dulunya adalah sel-sel kecil yang menjadi parasit dalam sel yang lebih besar. Kemudian, parasit-parasit ini kehilangan gen-gen yang tidak lagi dibutuhkan setelah hidup sebagai parasit. Dengan demikian, sel-sel tersebut mengalami regresi menjadi virus. Teori ini didukung oleh keberadaan bakteri seperti Rickettsia dan Chlamydia yang hanya mampu bereproduksi di dalam sel inang (seperti halnya virus). Menurut teori ini, jika sel-sel seperti ini bisa mengandalkan hidup sebagai parasit, gen-gen lain yang hanya diperlukan untuk hidup mandiri dapat hilang.
- Teori keluar dari sel
- Menurut teori ini, virus berevolusi dari potongan DNA atau RNA yang keluar dari gen organisme yang lebih besar. DNA yang keluar ini dapat berasal dari plasmid (potongan-potongan DNA yang dapat berpindah dari satu sel ke sel lain) dan juga dari bakteri.[27]
- Teori koevolusi
- Menurut teori ini, virus tidak berasal dari sel dan berevolusi dari molekul-molekul kompleks protein dan DNA pada saat yang sama dengan munculnya sel di bumi, dan selama bertahun-tahun selalu bergantung kepada sel hidup.[28]
Ketiga teori ini memiliki kelemahan. Teori regresi tidak dapat menjelaskan mengapa sel-sel parasit terkecil yang ditemukan pun tidak memiliki kemiripan sama sekali dengan virus. Teori keluar dari sel tidak dapat menjelaskan struktur-strukur yang hanya ada pada virus dan tidak pada sel. Teori koevolusi tidak dapat menjelaskan bagaimana virus yang terbentuk pertama kali dapat bertahan dan memperbanyak diri tanpa keberadaan sel.[28][29]
Mikrobiologi
Status kehidupan
Ada perbedaan pendapat ilmiah tentang apakah virus digolongkan sebagai makhluk hidup atau sekadar struktur organik yang berinteraksi dengan makhluk hidup. Walaupun demikian, mereka lebih sering dianggap sebagai replikator (zat yang melakukan replikasi DNA) dan tidak termasuk bentuk kehidupan.[30] Virus digambarkan sebagai "organisme di ujung kehidupan",[9] karena mereka serupa dengan makhluk hidup dalam hal kepemilikan gen, berevolusi melalui seleksi alam,[31] dan bereproduksi dengan membuat banyak salinan dari diri mereka sendiri melalui perakitan diri. Meskipun virus memiliki gen, mereka tidak memiliki sel, yang sering dipandang sebagai unit dasar kehidupan. Virus tidak memiliki metabolisme sendiri dan membutuhkan sel inang untuk membuat produk baru. Oleh karena itu, mereka tidak dapat bereproduksi secara alami di luar sel inang.[32] Walaupun sejumlah bakteri seperti Rickettsia dan Chlamydia memiliki keterbatasan yang sama, mereka dianggap sebagai organisme hidup karena memiliki sel sendiri.[33][34] Perakitan diri virus di dalam sel inang berimplikasi pada studi asal mula kehidupan karena mendukung hipotesis bahwa kehidupan dapat dimulai dari molekul organik yang dapat merakit diri.[35]
Struktur
Virus adalah organisme subseluler yang karena ukurannya sangat kecil, hanya dapat dilihat dengan menggunakan mikroskop elektron. Ukurannya lebih kecil daripada bakteri sehingga virus tidak dapat disaring dengan penyaring bakteri. Virus terkecil berdiameter hanya 20 nm (lebih kecil daripada ribosom), sedangkan virus terbesar sekalipun sukar dilihat dengan mikroskop cahaya.[36]
Genom virus dapat berupa DNA ataupun RNA.[37] Genom virus dapat terdiri dari DNA untai ganda, DNA untai tunggal, RNA untai ganda, atau RNA untai tunggal.[37] Selain itu, asam nukleat genom virus dapat berbentuk linear tunggal atau sirkuler.[37] Jumlah gen virus bervariasi dari empat untuk yang terkecil sampai dengan beberapa ratus untuk yang terbesar.[36][37] Bahan genetik kebanyakan virus hewan dan manusia berupa DNA, dan pada virus tumbuhan kebanyakan adalah RNA yang beruntai tunggal.[37]
Bahan genetik virus diselubungi oleh suatu lapisan pelindung.[37] Protein yang menjadi lapisan pelindung tersebut disebut kapsid.[37] Bergantung pada tipe virusnya, kapsid bisa berbentuk bulat (sferik), heliks, polihedral, atau bentuk yang lebih kompleks dan terdiri atas protein yang disandikan oleh genom virus.[37] Kapsid terbentuk dari banyak subunit protein yang disebut kapsomer.[36][37]
Untuk virus berbentuk heliks, protein kapsid (biasanya disebut protein nukleokapsid) terikat langsung dengan genom virus.[38] Misalnya, pada virus campak, setiap protein nukleokapsid terhubung dengan enam basa RNA membentuk heliks sepanjang sekitar 1,3 mikrometer.[38] Komposisi kompleks protein dan asam nukleat ini disebut nukleokapsid.[38] Pada virus campak, nukleokapsid ini diselubungi oleh lapisan lipid yang didapatkan dari sel inang, dan glikoprotein yang disandikan oleh virus melekat pada selubung lipid tersebut.[38] Bagian-bagian ini berfungsi dalam pengikatan pada dan pemasukan ke sel inang pada awal infeksi.[38]
Kapsid virus sferik menyelubungi genom virus secara keseluruhan dan tidak terlalu berikatan dengan asam nukleat seperti virus heliks.[39] Struktur ini bisa bervariasi dari ukuran 20 nanometer hingga 400 nanometer dan terdiri atas protein virus yang tersusun dalam bentuk simetri ikosahedral.[39] Jumlah protein yang dibutuhkan untuk membentuk kapsid virus sferik ditentukan dengan koefisien T, yaitu sekitar 60t protein.[39] Sebagai contoh, virus hepatitis B memiliki angka T=4, butuh 240 protein untuk membentuk kapsid.[39] Seperti virus bentuk heliks, kapsid sebagian jenis virus sferik dapat diselubungi lapisan lipid, namun biasanya protein kapsid sendiri langsung terlibat dalam penginfeksian sel.[39]
Beberapa jenis virus memiliki unsur tambahan yang membantunya menginfeksi inang.Virus pada hewan memiliki selubung virus, yaitu membran menyelubungi kapsid.[40] Selubung ini mengandung fosfolipid dan protein dari sel inang, tetapi juga mengandung protein dan glikoprotein yang berasal dari virus.[40] Selain protein selubung dan protein kapsid, virus juga membawa beberapa molekul enzim di dalam kapsidnya. Ada pula beberapa jenis bakteriofag yang memiliki ekor protein yang melekat pada "kepala" kapsid. Serabut-serabut ekor tersebut digunakan oleh fag untuk menempel pada suatu bakteri.[41] Partikel lengkap virus disebut virion. Virion berfungsi sebagai alat transportasi gen, sedangkan komponen selubung dan kapsid bertanggung jawab dalam mekanisme penginfeksian sel inang.[41]
Virus raksasa
Ilmuwan menemukan virus raksasa yang dikenal dengan istilah Mimivirus, Megavirus, dan Pandoravirus.
Pandoravirus merupakan jenis virus berukuran sangat besar dengan genom yang jauh lebih besar dibanding virus-virus lain yang sudah lebih dulu dikenal. Pandoravirus disebut sebagai virus super raksasa, karena ukurannya mengalahkan virus berukuran raksasa lain seperti Mimivirus atau Megavirus.
Meski berukuran raksasa, namun tetap tidak bisa dilihat dengan mata telanjang. Virus ini ditemukan peneliti dari Prancis Jean Michael Claverie dari Universitas Mediterranée.[42]
Pandoravirus berukuran seribu kali lebih besar dibanding virus influenza yang berukuran 100 nanometer. Pandoravirus memiliki 2.556 gen (200 kali lebih banyak dari virus influenza). Ukuran Pandoravirus lebih besar dua kali lipat dari Megavirus yang hanya memiliki 1.120 gen.
Replikasi
Replikasi virus terdiri atas beberapa tahapan-tahapan yaitu pelekatan virus, penetrasi, pelepasan mantel, replikasi genom dan ekspresi gen, perakitan, pematangan, dan pelepasan.
Pelekatan virus
Pelekatan virus (adsorpsi) merupakan proses interaksi awal antara partikel virus dengan molekul reseptor pada permukaan sel inang.[43] Pada tahap ini, terjadi ikatan spesifik antara molekul reseptor seluler dengan antireseptor pada virus.[43] Beberapa jenis virus memerlukan molekul lainnya untuk proses pelekatan yaitu koreseptor.[43]
Molekul reseptor yang target pada permukaan sel dapat berbentuk protein (biasanya glikoprotein) atau residu karbohidrat yang terdapat pada glikoprotein atau glikolipid.[43]
Beberapa virus kompleks seperti poxvirus dan herpesvirus memiliki lebih dari satu reseptor sehingga mempunyai beberapa rute untuk berikatan dengan sel.[43]
Reseptor virus mempunyai beberapa kelas yang berbeda:
- molekul immunoglobulin-like superfamily
- reseptor terkait membran
- saluran dan transporter transmembran[43]
Beberapa contoh virus beserta reseptor yang dimiliki:
- Human rhinovirus (HRV)
- Human rhinovirus memiliki reseptor ICAM-1(Intracelluler adhesion molecule-1).[44] Molekul tersebut merupakan molekul adhesi yang fungsi normalnya adalah untuk mengikatkan sel kepada substratnya.[44] struktur ICAM-1 mirip dengan molekul imunoglobulin dengan domain C dan V sehingga digolongkan sebagai protein supefamily immunoglobulin[44]
- Struktur ICAM-1 memiliki lima Ig-like domain untuk berikatan dengan Lfa-1 (Leukocite function antigen-1), Mac-1 (Macrofage antigen-1), Rhinovirus (HRV), fibrinogen, dan PFIE (malaria infected erythocytes).[44]
- Sepuluh serotipe dari HRV menggunakan ICAM-1 sebagai reseptor, sepuluh serotipe lainnya menggunakan protein yang beruhubungan dengan LDL reseptor.[44]
- Poliovirus
- Poliovirus mempunyai reseptor virus berupa protein membran integral yang juga anggota dari molekul superfamily immunoglobulin.[45] Reseptor ini memiliki tiga domain yaitu satu berupa variabel dan dua konstan.[45]
- Virus influenza
- Virus ini mempunyai dua tipe spike glikoprotein pada permukaan partikel virus yaitu hemagglutinin (HA) dan neuraminidase.[46] HA akan berikatan dengan reseptor virus influenza yang berupa asam sialat (N-asetil neuraminic acid).[46] Virus ini berikatan dengan muatan negatif dari moieties asam sialat yang ada pada rantai oligosakarida yang secara kovalen berikatan dengan glikoprotein pada permukaan sel.[46] Adanya asam sialat pada hampir semua jenis sel menyebabkan virus influenza bisa berikatan dengan banyak tipe sel.[46]
Penetrasi
Penetrasi terjadi pada waktu yang sangat singkat setelah pelekatan virus pada reseptor di membran sel.[47] Proses ini memerlukan energi Tiga mekanisme yang terlibat:
- Translokasi partikel virus
- Proses translokasi relatif jarang terjadi di antara virus dan mekanisme belum sepenuhnya dipahami benar, kemungkinan diperantarai oleh protein di dalam virus kapsid dan reseptor membran spesifik.[48]
- Endositosis virus ke dalam vakuola intraseluler
- Proses endositosis merupakan mekanisme yang sangat umum sebagai jalan masuk virus ke dalam sel.[49] Tidak diperlukan protein virus spesifik selain yang telah digunakan untuk pengikatan reseptor.[49]
- fusi dari sampul dengan membran sel (untuk virus yang bersampul)
- Proses fusi virus bersampul dengan membran sel baik secara langsung maupun dengan permukaan sel maupun mengikuti endositosis dalam sitoplasma.[49] Diperlukan adanya protein fusi spesifik dalam sampul virus, misalnya: HA influenza dan glikoprotein transmembran (TM) Rhinovirus.[49]
Pelepasan mantel
Tahap ini terjadi setelah proses penetrasi di mana kapsid virus baik seluruhnya maupun sebagian dipindahkan ke dalam sitoplasma sel inang.[47] Pada tahap ini genom virus terekspos dalam bentuk kompleks nukleoprotein.[47] Dalam beberapa kasus, tahap ini berlangsung cukup sederhana dan terjadi selama fusi pada membran virus dengan membran plasma.[47] untuk virus lainnya, tahap ini merupakan proses multistep yang melibatkan jalur endositosis dan membran nukleus.[47]
Replikasi genom dan ekspresi gen
Strategi replikasi dari beberapa virus tergantung pada material genetik alami dari virus tersebut.[51] Dalam hal ini, virus dibagi dalam 7 kelompok seperti pengelompokan David Baltimore.[51] Proses ekspresi gen akan menentukan semua proses infeksi virus (akut, kronis, persisten, atau laten).[51]
- Kelas I: DNA utas ganda
- Kelompok ini dibagi menjadi dua kelompok.
- Replikasi terjadi di inti dan relatif tergantung kepada faktor-faktor seluler (Adenoviridae, Polyomaviridae, Herpesviridae)[51]
- Replikasi terjadi di sitoplasma (Poxviridae). virus ini melibatkan semua faktor-faktor yang penting untuk transkripsi dan replikasi dari genomnya, dan kebanyakan tidak tergantung pada perangkat replikasi dari inangnya[51].
- Kelas II: DNA utas tunggal
- Replikasi terjadi di dalam nukleus, melibatkan bentuk utas ganda intermediate sebagai cetakan untuk sintesis utas tunggal DNA turunannya (Parvoviridae)[51]
- Kelas III: RNA utas ganda
- Virusnya memiliki genom yang tersegmentasi. masing-masing segmennya ditranskripsi secara terpisah untuk menghasilkan monosistronik mRNA individual. contoh: Reoviridae[51]
- Kelas IV: RNA utas tunggal (+)
- Virus dengan polisistronik mRNA di mana kelas ini genom RNA membentuk mRNA yang ditranslasikan untuk membentuk suatu polyprotein yang dipecah membentuk protein matang. Contoh: Picornaviridae[51]
- Kelas V: RNA utas tunggal (-)
- Genom pada kelas ini dibagi menjadi dua tipe:
- Genom tidak bersegmen (Rhabdoviridae), Tahap pertama dalam replikasi adalah transkripsi dari genom RNA utas (-) oleh virion RNA-dependent RNA polimerase untuk menghasilkan monosistronik mRNA yang juga sebagai cetakan untuk replikasi genom.[51]
- Genom bersegmen (Orthomyxoviridae), replikasi terjadi di dalam nukleus di mana monosistronik mRNA untuk masing-masing gen virus dihasilkan oleh transkriptase virus.[51]
- Kelas VI: RNA utas tunggal (+) dengan DNA Intermediat
- Genom Retrovirus RNA utas tunggal (+) bersifat diploid dan tidak dipakai secara langsung sebagai mRNA tetapi sebagi template untuk reverse transkriptase menjadi DNA.[51]
- Kelas VII: DNA utas ganda dengan RNA Intermediat
- Virus kelompok ini bergantung kepada reverse transkriptase, tetapi berbeda dengan retrovirus, prosesnya terjadi di dalam partikel virus selama maturasi (Hepadnaviridae).[51]
Perakitan
Perakitan merupakan proses pengumpulan komponen-komponen virion pada bagian khusus di dalam sel.[47] Selama proses ini, terjadi pembentukan struktur partikel virus.[47] Proses ini tergantung kepada proses replikasi di dalam sel dan tempat di mana virus melepaskan diri dari sel.[47] mekanisme perakitan bervariasi untuk virus yang berbeda-beda. Contoh: proses perakitan Picornavirus, Poxvirus, dan Reovirus terjadi di sitoplasma, sementara itu proses perakitan Adenovirus, Poliovirus, dan Parvovirus terjadi di nukleus.[47]
Pematangan
Pematangan merupakan tahap dari siklus hidup virus dan bersifat infeksius.[47] Pada tahap ini terjadi perubahan struktur dalam partikel virus yang kemungkinan dihasilkan oleh pemecahan spesifik protein kapsid untuk menghasilkan produk yang matang.[47] protease virus dan enzim seluler lainnya biasanya terlibat dalam proses ini.[47]
Pelepasan
Semua virus kecuali virus tanaman melepaskan diri dari sel inang melalui dua mekanisme:
- untuk virus litik (semua virus non-selubung), pelepasan merupakan proses yang sederhana, di mana sel yang terinfeksi terbuka dan virus keluar.[47]
- untuk virus berselubung, diperlukan membran lipid ketika virus keluar dari sel melewati membran, proses ini dikenal sebagai budding.[47]
Proses pelepasan partikel virus kemungkinan bisa merusak sel(Paramyxovirus, Rhabdovirus, dan Togavirus), dan kemungkinan sebagian lagi tidak merusak sel (Retrovirus).[47]
Klasifikasi
Klasifikasi bertujuan untuk menggambarkan keanekaragaman virus dengan memberi nama dan mengelompokkan virus berdasarkan kesamaan mereka. Secara sederhana, virus dapat dikelompokkan berdasarkan jenis asam nukleat yang mereka miliki (virus DNA atau virus RNA), untaian asam nukleat (untai tunggal atau untai ganda), ada tidaknya segmentasi pada genom, ukuran virion, jenis simetri kapsid (heliks atau ikosahedreal), serta ada tidaknya selubung.[52] Pada tahun 1962, André Lwoff, Robert Horne, dan Paul Tournier merupakan orang-orang pertama yang mengembangkan pengelompokan virus berdasarkan sistem hierarki Linnaeus.[53] Sistem ini menggunakan klasifikasi filum, kelas, bangsa, keluarga, marga, dan spesies. Virus dikelompokkan sesuai dengan kesamaan sifat mereka (bukan kesamaan inang mereka) dan jenis asam nukleat yang membentuk genom mereka.[54] Pada tahun 1966, Komite Internasional Taksonomi Virus (ICTV) dibentuk. Sistem yang diusulkan oleh Lwoff, Horne, dan Tournier tidak pernah sepenuhnya diterima oleh ICTV karena ukuran genom virus yang kecil dan tingkat mutasi mereka yang tinggi membuat sulit untuk menentukan takson virus di atas ordo (bangsa). Oleh sebab itu, klasifikasi Baltimore digunakan untuk melengkapi hierarki yang lebih tradisional.[55] Mulai tahun 2018, ICTV mulai mengakui hubungan evolusi yang lebih dalam di antara virus yang telah ditemukan dan mengadopsi sistem klasifikasi dengan 15 tingkatan, mulai dari dunia hingga spesies.[56]
Klasifikasi ICTV
Komite Internasional Taksonomi Virus (ICTV) mengembangkan sistem klasifikasi yang digunakan saat ini dan menulis pedoman yang memberi bobot lebih besar pada sifat-sifat virus tertentu untuk menjaga keseragaman keluarga virus. Taksonomi terpadu (sistem universal untuk mengklasifikasikan virus) telah ditetapkan. Peneliti baru mendeskripsikan sebagian kecil dari total keragaman virus yang ada di bumi.[57] Pada tahun 2019, 4 dunia, 9 kerajaan, 16 filum, 2 subfilum, 36 kelas, 55 ordo, 8 subordo, 168 keluarga, 103 subkeluarga, 1.421 genus, 68 subgenus, dan 6.589 spesies virus telah ditetapkan oleh ICTV.[58]
Seperti taksonomi makhluk hidup pada umumnya, klasifikasi virus juga dilakukan secara hierarkis atau bertingkat. Pada 2019, tingkatan subdunia, subkerajaan, dan subkelas tidak digunakan, sedangkan semua tingkatan lainnya sedang digunakan.
- Dunia (-viria)
Dalam klasifikasi virus, terdapat pula takson yang dikategorikan sebagai incertae sedis atau penempatannya tidak pasti.
Klasifikasi Baltimore
Ahli biologi dan pemenang Hadiah Nobel David Baltimore merancang sistem klasifikasi Baltimore.[59][60] Dalam klasifikasi virus modern, sistem klasifikasi ICTV digunakan bersama dengan sistem klasifikasi Baltimore.[61][62][63]
Klasifikasi virus Baltimore didasarkan pada mekanisme sintesis mRNA. Virus harus menghasilkan mRNA dari genomnya untuk menghasilkan protein dan mereplikasi diri mereka sendiri, tetapi mekanisme yang digunakan oleh virus untuk mencapai hal ini berbeda-beda. Genom virus mungkin beruntai tunggal (single-stranded, disingkat ss) atau beruntai ganda (double-stranded, disingkat ds), baik berupa RNA atau DNA, dan mungkin menggunakan atau tidak menggunakan transkriptase balik (reverse transcriptase, disingkat RT). Selain itu, virus RNA untai tunggal dapat bersifat positif (+) atau negatif (-). Klasifikasi ini menempatkan virus ke dalam tujuh kelompok:
- Virus DNA untai ganda (dsDNA)
- Virus DNA untai tunggal (ssDNA)
- Virus RNA untai ganda (dsRNA)
- Virus RNA untai tunggal-positif (ssRNA(+))
- Virus RNA untai tunggal-negatif (ssRNA(-))
- Virus RNA untai tunggal-transkripsi balik (ssRNA-RT)
- Virus DNA untai ganda-transkripsi balik (dsDNA-RT)
Sebagai contoh penerapan klasifikasi virus, virus penyebab cacar air, yaitu virus varicella-zoster (VZV), ditempatkan dalam ordo Herpesvirales, keluarga Herpesviridae, subkeluarga Alphaherpesvirinae, dan genus Varicellovirus. VZV berada di Grup I dari Klasifikasi Baltimore karena merupakan virus dsDNA yang tidak menggunakan enzim transkriptase balik.
Set lengkap virus dalam suatu organisme atau habitat disebut viroma; misalnya, semua virus manusia membentuk viroma manusia.[64]
Virus dan penyakit
Infeksi virus pada sel inang dapat menimbulkan penyakit yang dikategorikan sebagai penyakit infeksius. Penyebaran virus dari satu inang ke inang lain bisa dilakukan dengan banyak cara, tetapi setiap virus memiliki karakteristik tertentu dan mengandalkan cara tertentu untuk menyebar. Banyak virus yang menginfeksi tumbuhan berpindah dari satu tumbuhan ke tumbuhan lain melalui serangga dan organisme lain yang disebut vektor.[65] Virus yang menginfeksi hewan dan manusia menyebar dengan berbagai cara. Beberapa virus berpindah melalui kontak langsung antara individu terinfeksi dengan individu sehat, misalnya herpes simpleks yang menular melalui sentuhan fisik.[66] Penularan virus melalui kontak langsung juga dapat terjadi melalui hubungan seks, misalnya HIV.[67] Virus yang menginfeksi saluran pencernaan, seperti Norovirus dan Rotavirus, ditularkan melalui transmisi fekal–oral, yang melibatkan tangan, makanan, dan minuman yang terkontaminasi.[68][69] Virus-virus yang menyerang sistem pernapasan, seperti virus influenza, virus parainfluenza, dan virus korona, dapat menyebar melalui percikan dari saluran pernapasan saat seseorang berbicara, batuk, atau bersin.[70][71][72] Apabila partikel virus dalam percikan tersebut berhasil menyentuh membran mukosa orang lain (yang ada di hidung, mulut, dan beberapa organ lain), mereka dapat masuk ke dalam tubuh individu tersebut. Virus lainnya, seperti virus dengue, disebarkan oleh serangga pengisap darah.[73] Sementara itu, Cytomegalovirus bisa diturunkan secara vertikal dari ibu hamil ke janin yang sedang dikandungnya.[74]
Dampak
Beberapa virus ada yang dapat dimanfaatkan dalam rekombinasi genetika.[75] Melalui terapi gen, gen jahat (penyebab infeksi) yang terdapat dalam virus diubah menjadi gen baik (penyembuh).[75] Baru-baru ini David Sanders, seorang profesor biologi pada Purdue's School of Science telah menemukan cara pemanfaatan virus dalam dunia kesehatan.[75] Dalam temuannva yang dipublikasikan dalam Jurnal Virology, Edisi 15 Desember 2002, David Sanders berhasil menjinakkan cangkang luar virus Ebola sehingga dapat dimanfaatkan sebagai pembawa gen kepada sel yang sakit (paru-paru).[75] Meskipun demikian, kebanyakan virus bersifat merugikan terhadap kehidupan manusia, hewan, dan tumbuhan.[75]
Virus sangat dikenal sebagai penyebab penyakit infeksi pada manusia, hewan, dan tumbuhan.[75] Sejauh ini tidak ada makhluk hidup yang tahan terhadap virus.[75] Tiap virus secara khusus menyerang sel-sel tertentu dari inangnya. Virus yang menyebabkan selesma menyerang saluran pernapasan, virus campak menginfeksi kulit, virus hepatitis menginfeksi hati, dan virus rabies menyerang sel-sel saraf. Begitu juga yang terjadi pada penyakit AIDS (acquired immune deficiency syndrome), yaitu suatu penyakit yang mengakibatkan menurunnya daya tahan tubuh penderita penyakit tersebut disebabkan oleh virus HIV yang secara khusus menyerang sel darah putih.[75] Tabel berikut ini memuat beberapa macam penyakit yang disebabkan oleh virus.[75]
Selain manusia, virus juga menyebabkan kesengsaraan bagi hewan dan tumbuhan.[75] Tidak sedikit pula kerugian yang diderita peternak atau petani akibat ternaknya yang sakit atau hasil panennya yang berkurang.[75]
Penyakit hewan akibat virus
Penyakit tetelo, yakni jenis penyakit yang menyerang bangsa unggas, terutama ayam. Penyebabnya adalah new castle disease virus (NCDV).[75] Penyakit kuku dan mulut, yakni jenis penyakit yang menyerang ternak sapi dan kerbau.[75] Penyakit kanker pada ayam oleh rous sarcoma virus (RSV).[75] Penyakit rabies, yakni jenis penyakit yang menyerang anjing, kucing, dan monyet, disebabkan oleh virus rabies.[75]
Penyakit tumbuhan akibat virus
Penyakit mosaik, yakni jenis penyakit yang menyerang tanaman tembakau.[15] Penyebabnya adalah tobacco mosaic virus (TMV) Penyakit tungro, yakni jenis penyakit yang menyerang tanaman padi.[15] Penyebabnya adalah virus Tungro.[15] Penyakit degenerasi pembuluh tapis pada jeruk. Penyebabnya adalah virus citrus vein phloem degeneration (CVPD).[15]
Penyakit manusia akibat virus
Contoh paling umum dari penyakit yang disebabkan oleh virus adalah pilek (yang bisa saja disebabkan oleh satu atau beberapa virus sekaligus), cacar, AIDS (yang disebabkan virus HIV), dan demam herpes (yang disebabkan virus herpes simpleks).[76] Kanker leher rahim juga diduga disebabkan sebagian oleh papilomavirus (yang menyebabkan papiloma, atau kutil), yang memperlihatkan contoh kasus pada manusia yang memperlihatkan hubungan antara kanker dan agen-agen infektan.[76] Juga ada beberapa kontroversi mengenai apakah virus borna, yang sebelumnya diduga sebagai penyebab penyakit saraf pada kuda, juga bertanggung jawab kepada penyakit psikiatris pada manusia.[76]
Potensi virus untuk menyebabkan wabah pada manusia menimbulkan kekhawatiran penggunaan virus sebagai senjata biologis. Kecurigaan meningkat seiring dengan ditemukannya cara penciptaan varian virus baru di laboratorium.[76]
Kekhawatiran juga terjadi terhadap penyebaran kembali virus sejenis cacar, yang telah menyebabkan wabah terbesar dalam sejarah manusia, dan mampu menyebabkan kepunahan suatu bangsa.[76] Beberapa suku bangsa Indian telah punah akibat wabah, terutama penyakit cacar, yang dibawa oleh kolonis Eropa.[76] Meskipun sebenarnya diragukan dalam jumlah pastinya, diyakini kematian telah terjadi dalam jumlah besar.[76] Penyakit ini secara tidak langsung telah membantu dominasi bangsa Eropa di dunia baru Amerika.[76]
Salah satu virus yang dianggap paling berbahaya adalah filovirus.[76] Grup Filovirus terdiri atas Marburg, pertama kali ditemukan tahun 1967 di Marburg, Jerman, dan ebola.[76] Filovirus adalah virus berbentuk panjang seperti cacing, yang dalam jumlah besar tampak seperti sepiring mi.[76] Pada April 2005, virus Marburg menarik perhatian pers dengan terjadinya penyebaran di Angola. Sejak Oktober 2004 hingga 2005, kejadian ini menjadi epidemi terburuk di dalam kehidupan manusia.[76]
Diagnosis di laboratorium
Deteksi, isolasi, hingga analisis suatu virus biasanya melewati proses yang sulit dan mahal.[77] Karena itu, penelitian penyakit akibat virus membutuhkan fasilitas besar dan mahal, termasuk juga peralatan yang mahal dan tenaga ahli dari berbagai bidang, misalnya teknisi, ahli biologi molekular, dan ahli virus.[77] Biasanya proses ini dilakukan oleh lembaga kenegaraan atau dilakukan secara kerjasama dengan bangsa lain melalui lembaga dunia seperti Organisasi Kesehatan Dunia (WHO).[77]
Pencegahan dan pengobatan
Karena biasanya memanipulasi mekanisme sel induknya untuk bereproduksi, virus sangat sulit untuk dibunuh.[78] Metode pengobatan sejauh ini yang dianggap paling efektif adalah vaksinasi, untuk merangsang kekebalan alami tubuh terhadap proses infeksi, dan obat-obatan yang mengatasi gejala akibat infeksi virus.[78]
Penyembuhan penyakit akibat infeksi virus biasanya disalah-antisipasikan dengan penggunaan antibiotik, yang sama sekali tidak mempunyai pengaruh terhadap kehidupan virus.[78] Efek samping penggunaan antibiotik adalah resistansi bakteri terhadap antibiotik.[78] Karena itulah diperlukan pemeriksaan lebih lanjut untuk memastikan apakah suatu penyakit disebabkan oleh bakteri atau virus.[78]
Infeksi virus atau bakteri pada umumnya menimbulkan demam, hanya saja infeksi bakteri akan meningkatkan kadar Sel darah putih, sedangkan infeksi virus tidak, tetapi infeksi bakteri, virus bahkan jamur akan meningkatkan kadar Antibodi M (IgM), tetapi pemeriksaan IgM agak mahal. Pemeriksaan Sel darah putih ataupun IgM tidak dapat menentukan jenis penyakitnya, tetapi kedua pemeriksaan tersebut hanya mengindikasikan penyakit tersebut diakibatkan oleh apa. Jika biaya menjadi kendala, maka pemeriksaan Sel darah putih saja sudah cukup, karena infeksi virus tidak dapat diobati dengan anti-biotik dan pada umumnya infeksi virus akan sembuh dengan sendirinya (virus self limiting life) dengan istirahat (istirahat penuh di ranjang, jika perlu) dan gizi yang cukup, kecuali HIV di mana untuk diagnosis awal diperlukan pemeriksaan CD4 yang relatif murah.
Lihat pula
Referensi
Catatan kaki
- ^ a b "Virus Taxonomy: 2019 Release". ICTV Online. Juli 2019. Diakses tanggal 7 Oktober 2020.
- ^ Koonin, Eugene V.; Senkevich, Tatiana G.; Dolja, Valerian V. (2006-09-19). "The ancient Virus World and evolution of cells". Biology Direct. 1: 29. doi:10.1186/1745-6150-1-29. ISSN 1745-6150. PMC 1594570 . PMID 16984643.
- ^ Dimmock, hlm. 4.
- ^ Breitbart M, Rohwer F (Juni 2005). "Here a virus, there a virus, everywhere the same virus?". Trends in Microbiology. 13 (6): 278–284. doi:10.1016/j.tim.2005.04.003. PMID 15936660.
- ^ Lawrence CM, Menon S, Eilers BJ, Bothner B, Khayat R, Douglas T, Young MJ (May 2009). "Structural and functional studies of archaeal viruses". The Journal of Biological Chemistry. 284 (19): 12599–603. doi:10.1074/jbc.R800078200. PMC 2675988 . PMID 19158076.
- ^ Edwards RA, Rohwer F (June 2005). "Viral metagenomics". Nature Reviews. Microbiology. 3 (6): 504–10. doi:10.1038/nrmicro1163. PMID 15886693.
- ^ Canchaya, Carlos; Fournous, Ghislain; Chibani-Chennoufi, Sandra; Dillmann, Marie-Lise; Brüssow, Harald (Agustus 2003). "Phage as agents of lateral gene transfer". Current Opinion in Microbiology. 6 (4): 417–424. doi:10.1016/S1369-5274(03)00086-9. PMID 12941415.
- ^ a b Koonin, Eugene V.; Starokadomskyy, Petro (Oktober 2016). "Are viruses alive? The replicator paradigm sheds decisive light on an old but misguided question". Studies in History and Philosophy of Science Part C: Studies in History and Philosophy of Biological and Biomedical Sciences. 59: 125–134. doi:10.1016/j.shpsc.2016.02.016. PMC 5406846 . PMID 26965225.
- ^ a b Rybicki, E. (April 1990). "The classification of organisms at the edge of life or problems with virus systematics" (PDF). South African Journal of Science. 86: 182–186.
- ^ Robilotti, Elizabeth; Deresinski, Stan; Pinsky, Benjamin A. (Januari 2015). "Norovirus". Clinical Microbiology Reviews. 28 (1): 134–164. doi:10.1128/CMR.00075-14. ISSN 0893-8512. PMC 4284304 . PMID 25567225.
- ^ Shors, hlm. 123–124.
- ^ a b "virus (n.)". Etymonline. Diakses tanggal 8 April 2020.
- ^ "virulent (adj.)". Etymonline. Diakses tanggal 8 April 2020.
- ^ "viral (adj.)". Etymonline. Diakses tanggal 8 April 2020.
- ^ a b c d e f g h Akin, H.M. (2005). Virologi Tumbuhan (Didigitalisasi oleh Google Penelusuran Buku). Yogyakarta: Kanisius. hlm. hlm. 17. ISBN 9792111808, 9789792111804 Periksa nilai: invalid character
|isbn=(bantuan). Diakses tanggal 2009-03-13. - ^ Campbell et al. (2002), hlm. 341. Diakses pada 26 Maret 2009.
- ^ Stanley WM (1933). "Isolation of a crystalline protein possessing the properties of tobacco mosaic virus" (pdf). Science. 81: 644–645.
- ^ Creager, A.N.H. (2002). The life of a virus: tobacco mosaic virus as an experimental model, 1930-1965 (Didigitalisasi oleh Google Penelusuran Buku) (edisi ke-Edisi ke-2). Chicago: University of Chicago Press. hlm. hlm. 119. ISBN 0226120260, 9780226120263 Periksa nilai: invalid character
|isbn=(bantuan). Diakses tanggal 2009-03-26. - ^ a b c d Rous P (1911). "A sarcoma of the fowl transmissible by an agent separable from the tumor cells" (pdf). J Exp Med. 13: 397–399.
- ^ a b Shope RE (1933). "Infectious papillomatosis of rabbits; with a note on the histopathology" (pdf). J Exp Med. 58: 607.
- ^ a b Hershey AD, Chase M (1952). "Independent Function of Viral Protein and Nucleic Acid in Growth of Bacteriophage" (pdf). Journal of General Physiology. 36: 39–56.
- ^ Shors 2017, hlm. 16.
- ^ Collier dkk. 1998, hlm. 18–19.
- ^ Liu Y, Nickle DC, Shriner D, Jensen MA, Learn GH, Mittler JE, Mullins JI (November 2004). "Molecular clock-like evolution of human immunodeficiency virus type 1". Virology. 329 (1): 101–08. doi:10.1016/j.virol.2004.08.014. PMID 15476878.
- ^ a b Krupovic M, Dooja W, Koonin EV (2019). "Origin of viruses: primordial replicators recruiting capsids from hosts". Nature Reviews Microbiology. 17 (7): 449–58. doi:10.1038/s41579-019-0205-6. PMID 31142823.
- ^ Collier dkk. 1998, hlm. 11–21.
- ^ Collier dkk. 1998, hlm. 11–12.
- ^ a b Wessner DR (2010). "The Origins of Viruses". Nature Education. 3 (9): 37.
- ^ Nasir A, Kim KM, Caetano-Anollés G (2012). "Viral evolution: Primordial cellular origins and late adaptation to parasitism". Mobile Genetic Elements. 2 (5): 247–52. doi:10.4161/mge.22797. PMID 23550145.
- ^ Koonin, E.V.; Starokadomskyy, P. (7 Maret 2016). "Are viruses alive? The replicator paradigm sheds decisive light on an old but misguided question". Stud Hist Philos Biol Biomed Sci. 59: 125–34. doi:10.1016/j.shpsc.2016.02.016. PMC 5406846 . PMID 26965225.
- ^ Holmes EC (October 2007). "Viral evolution in the genomic age". PLOS Biology. 5 (10): e278. doi:10.1371/journal.pbio.0050278. PMC 1994994 . PMID 17914905.
- ^ Wimmer E, Mueller S, Tumpey TM, Taubenberger JK (December 2009). "Synthetic viruses: a new opportunity to understand and prevent viral disease". Nature Biotechnology. 27 (12): 1163–72. doi:10.1038/nbt.1593. PMC 2819212 . PMID 20010599.
- ^ Horn M (2008). "Chlamydiae as symbionts in eukaryotes". Annual Review of Microbiology. 62: 113–31. doi:10.1146/annurev.micro.62.081307.162818. PMID 18473699.
- ^ Ammerman NC, Beier-Sexton M, Azad AF (November 2008). "Laboratory maintenance of Rickettsia rickettsii". Current Protocols in Microbiology. Chapter 3 (1): Unit 3A.5. doi:10.1002/9780471729259.mc03a05s11. ISBN 978-0471729259. PMC 2725428 . PMID 19016440.
- ^ Koonin EV, Senkevich TG, Dolja VV (September 2006). "The ancient Virus World and evolution of cells". Biology Direct. 1 (1): 29. doi:10.1186/1745-6150-1-29. PMC 1594570 . PMID 16984643.
- ^ a b c Campbell et al. (2002), hlm. 342. Diakses pada 26 Maret 2009.
- ^ a b c d e f g h i Wagner (2008), Basic Virology, Australia: Blackwell Publishing, ISBN 2007019839 Periksa nilai: checksum
|isbn=(bantuan) (lihat di Penelusuran Buku Google) - ^ a b c d e Wagner (2008), Basic Virology, Australia: Blackwell Publishing, ISBN 2007019839 Periksa nilai: checksum
|isbn=(bantuan) (lihat di Penelusuran Buku Google) - ^ a b c d e Mahy, BWJ.; van Regenmortel, MHW. (2010), Desk Encyclopedia of General Virology, San Diego: Elsevier, ISBN 978-0-12-375145-1 Periksa nilai: checksum
|isbn=(bantuan) (lihat di Penelusuran Buku Google) - ^ a b Mahy, BWJ.; van Regenmortel, MHW. (2010), Desk Encyclopedia of General Virology, San Diego: Elsevier, ISBN 978-0-12-375145-1 Periksa nilai: checksum
|isbn=(bantuan) (lihat di Penelusuran Buku Google) - ^ a b Strauss, JH.; Strauss, EG. (2008), Viruses and Human Disease, London: Elsevier, ISBN 978-0-12-375145-1 Periksa nilai: checksum
|isbn=(bantuan) (lihat di Penelusuran Buku Google) - ^ Pandoravirus, Virus Super Raksasa PortalKBR, 22 Juli 2013
- ^ a b c d e f Schneider-Schaulies J (2000). "Cellular receptors for viruses: links to tropism and pathogenesis" (pdf). Journal of General Virology. 81: 1413–1429.
- ^ a b c d e Olson NH (1992). "Structure of a human rhinovirus complexed with its receptormolecule" (pdf). Proc. Natl. Acad. Sci. USA. 90: 507–511.
- ^ a b Yongning H. (2000). "Interaction of the poliovirus receptor with poliovirus" (pdf). PNAS. 97: 79–84.
- ^ a b c d Hidari KIPJ (2010). "Glycan Receptor for Influenza Virus" (pdf). The Open Antimicrobial Agents Journal. 2: 26–33.
- ^ a b c d e f g h i j k l m n o Mahy, BWJ.; van Regenmortel, MHW. (2010), Desk Encyclopedia of General Virology, San Diego: Elsevier, ISBN 978-0-12-375145-1 Periksa nilai: checksum
|isbn=(bantuan) (lihat di Penelusuran Buku Google) - ^ Cossart, P (2005), Cellular Microbiology, Washington DC: American Society for Microbiology Press, ISBN 1-55581-302-X (lihat di Penelusuran Buku Google)
- ^ a b c d Cheng, H.; Hammar, L. (2004), Cellular Microbiology, Singapore: World Scientifis Publishing Co. Pte. Ltd., ISBN 981-238-614-9 (lihat di Penelusuran Buku Google)
Kesalahan pengutipan: Tanda
<ref>tidak sah; nama "Cheng" didefinisikan berulang dengan isi berbeda - ^ Carter, JB.; Saunders, VA. (2007), Virology: Principles and Applications, England: John Wiley & Sons, Ltd., ISBN 978-0-470-023860-0 Periksa nilai: length
|isbn=(bantuan) (lihat di Penelusuran Buku Google) - ^ a b c d e f g h i j k l Wagner (2008), Basic Virology, Australia: Blackwell Publishing, ISBN 2007019839 Periksa nilai: checksum
|isbn=(bantuan) (lihat di Penelusuran Buku Google) - ^ Carter & Saunders 2007, hlm. 116.
- ^ Lwoff A, Horne RW, Tournier P (June 1962). "[A virus system]". Comptes Rendus Hebdomadaires des Seances de l'Academie des Sciences (dalam bahasa French). 254: 4225–7. PMID 14467544.
- ^ Lwoff A, Horne R, Tournier P (1962). "A system of viruses". Cold Spring Harbor Symposia on Quantitative Biology. 27: 51–5. doi:10.1101/sqb.1962.027.001.008. PMID 13931895.
- ^ Fauquet CM, Fargette D (August 2005). "International Committee on Taxonomy of Viruses and the 3,142 unassigned species". Virology Journal. 2: 64. doi:10.1186/1743-422X-2-64. PMC 1208960 . PMID 16105179.
- ^ International Committee on Taxonomy of Viruses Executive Committee (Mei 2020). "The New Scope of Virus Taxonomy: Partitioning the Virosphere Into 15 Hierarchical Ranks". Nat Microbiol. 5 (5): 668–674. doi:10.1038/s41564-020-0709-x. PMC 7186216 . PMID 32341570.
- ^ Delwart EL (2007). "Viral metagenomics". Reviews in Medical Virology. 17 (2): 115–31. doi:10.1002/rmv.532. PMID 17295196.
- ^ "Virus Taxonomy: 2019 Release". ICTV Online. Juli 2019. Diakses tanggal 7 Oktober 2020.
- ^ Temin HM, Baltimore D (1972). "RNA-directed DNA synthesis and RNA tumor viruses". Advances in Virus Research. 17: 129–86. doi:10.1016/S0065-3527(08)60749-6. ISBN 9780120398171. PMID 4348509.
- ^ Baltimore D (1974). "The strategy of RNA viruses". Harvey Lectures. 70 Series: 57–74. PMID 4377923.
- ^ van Regenmortel MH, Mahy BW (January 2004). "Emerging issues in virus taxonomy". Emerging Infectious Diseases. 10 (1): 8–13. doi:10.3201/eid1001.030279. PMC 3322749 . PMID 15078590.
- ^ Mayo MA (1999). "Developments in plant virus taxonomy since the publication of the 6th ICTV Report. International Committee on Taxonomy of Viruses". Archives of Virology. 144 (8): 1659–66. doi:10.1007/s007050050620. PMID 10486120.
- ^ de Villiers EM, Fauquet C, Broker TR, Bernard HU, zur Hausen H (June 2004). "Classification of papillomaviruses". Virology. 324 (1): 17–27. doi:10.1016/j.virol.2004.03.033. PMID 15183049.
- ^ Parker MT (September 2016). "An Ecological Framework of the Human Virome Provides Classification of Current Knowledge and Identifies Areas of Forthcoming Discovery". The Yale Journal of Biology and Medicine. 89 (3): 339–351. PMC 5045143 . PMID 27698618.
- ^ Dietzgen, Ralf; Mann, Krin; Johnson, Karyn (9 November 2016). "Plant Virus–Insect Vector Interactions: Current and Potential Future Research Directions". Viruses (dalam bahasa Inggris). 8 (11): 303. doi:10.3390/v8110303. ISSN 1999-4915. PMC 5127017 . PMID 27834855.
- ^ "Herpes simplex virus". WHO (dalam bahasa Inggris). Diakses tanggal 8 April 2020.
- ^ Shaw, G. M.; Hunter, E. (1 November 2012). "HIV Transmission". Cold Spring Harbor Perspectives in Medicine (dalam bahasa Inggris). 2 (11): a006965–a006965. doi:10.1101/cshperspect.a006965. ISSN 2157-1422. PMC 3543106 . PMID 23043157.
- ^ Gaythorpe, K. A. M.; Trotter, C. L.; Lopman, B.; Steele, M.; Conlan, A. J. K. (Januari 2018). "Norovirus transmission dynamics: a modelling review". Epidemiology and Infection (dalam bahasa Inggris). 146 (2): 147–158. doi:10.1017/S0950268817002692. ISSN 0950-2688. PMC 5851036 . PMID 29268812.
- ^ Crawford, Sue E.; Ramani, Sasirekha; Tate, Jacqueline E.; Parashar, Umesh D.; Svensson, Lennart; Hagbom, Marie; Franco, Manuel A.; Greenberg, Harry B.; O'Ryan, Miguel (Desember 2017). "Rotavirus infection". Nature Reviews Disease Primers (dalam bahasa Inggris). 3 (1): 17083. doi:10.1038/nrdp.2017.83. ISSN 2056-676X. PMC 5858916 . PMID 29119972.
- ^ Neumann, Gabriele; Kawaoka, Yoshihiro (Mei 2015). "Transmission of influenza A viruses". Virology (dalam bahasa Inggris). 479-480: 234–246. doi:10.1016/j.virol.2015.03.009. PMC 4424116 . PMID 25812763.
- ^ Burke, Crystal W.; Bridges, Olga; Brown, Sherri; Rahija, Richard; Russell, Charles J. (21 November 2013). Subbarao, Kanta, ed. "Mode of Parainfluenza Virus Transmission Determines the Dynamics of Primary Infection and Protection from Reinfection". PLoS Pathogens (dalam bahasa Inggris). 9 (11): e1003786. doi:10.1371/journal.ppat.1003786. ISSN 1553-7374. PMC 3836739 . PMID 24278024.
- ^ Singhal, Tanu (April 2020). "A Review of Coronavirus Disease-2019 (COVID-19)". The Indian Journal of Pediatrics (dalam bahasa Inggris). 87 (4): 281–286. doi:10.1007/s12098-020-03263-6. ISSN 0019-5456. PMC 7090728 . PMID 32166607.
- ^ Marques-Toledo, Cecilia A.; Bendati, Maria Mercedes; Codeço, Claudia T.; Teixeira, Mauro M. (Desember 2019). "Probability of dengue transmission and propagation in a non-endemic temperate area: conceptual model and decision risk levels for early alert, prevention and control". Parasites & Vectors (dalam bahasa Inggris). 12 (1): 38. doi:10.1186/s13071-018-3280-z. ISSN 1756-3305. PMC 6335707 . PMID 30651125.
- ^ Britt, William (3 Agustus 2018). "Maternal Immunity and the Natural History of Congenital Human Cytomegalovirus Infection". Viruses (dalam bahasa Inggris). 10 (8): 405. doi:10.3390/v10080405. ISSN 1999-4915. PMC 6116058 . PMID 30081449.
- ^ a b c d e f g h i j k l m n o Evans, AS.; Kaslow, RA. (1997), Viral Infections of Humans:epidemiology and Control, New York: Plenum Publishing Corporation, ISBN 0-306-44856-4 (lihat di Penelusuran Buku Google)
- ^ a b c d e f g h i j k l Crowley, LV. (2010), An Introduction to Human Disease: Pathology and Pathophysiology, Sudburry: Jones and Bartlett Publishers, ISBN 978-0-7637-6591-0 (lihat di Penelusuran Buku Google)
- ^ a b c Zuckerman, AJ.; Banatvala, JE.; Griffiths, P. (2009), Principles and Practice of Clinical Virology, England: John Wiley & Sons Ltd., ISBN 978-0-470-51799-4 (lihat di Penelusuran Buku Google)
- ^ a b c d e Singh, M. (2007), Vaccine Adjuvants and Delivery Systems, New Jersey: John Wiley & Sons Ltd., ISBN 978-0-471-73907-4 (lihat di Penelusuran Buku Google)
Daftar pustaka
- Carter, John B.; Saunders, Venetia A. (2007). Virology: Principles and Applications. Chichester, Inggris: John Wiley & Sons. ISBN 978-0-470-02386-0. OCLC 124160564.
- Collier, Leslie; Balows, Albert; Sussman, Max, ed. (1998). Topley and Wilson's Microbiology and Microbial Infections (edisi ke-9). London: Arnold. ISBN 0-340-61470-6. OCLC 38290809.
- Hörnlimann, Beat (2006). Prions in Humans and Animals. Berlin: Walter de Gruyter. ISBN 978-3-11-020017-1. OCLC 712015585.
- Organisasi Kesehatan Dunia (2004). "Annex 4. Guidelines on Viral Inactivation and Removal Procedures Intended to Assure the Viral Safety of Human Blood Plasma Products" (PDF). WHO Expert Commitee on Biological Standardization. WHO Technical Report No. 924: Fifty-second report. Jenewa: Organisasi Kesehatan Dunia.
- Shors, Teri (2017). Understanding Viruses (edisi ke-3). Burlington, Massachusetts: Jones and Bartlett Learning. ISBN 978-1-284-02592-7. OCLC 948427269.
Pranala luar
- (Inggris) Perpustakaan Online tentang virus
- (Inggris) Wong's Virology
- (Inggris) Apa itu virus?