Siklus asam sitrat
Siklus asam sitrat[1] (bahasa Inggris: citric acid cycle, tricarboxylic acid cycle, TCA cycle, Krebs cycle, Szent-Györgyi-Krebs cycle) adalah sederetan jenjang reaksi metabolisme pernapasan selular yang terpacu enzim yang terjadi setelah proses glikolisis, dan bersama-sama merupakan pusat dari sekitar 500 reaksi metabolisme yang terjadi di dalam sel.[2] Lintasan katabolisme akan menuju pada lintasan ini dengan membawa molekul kecil untuk diiris guna menghasilkan energi, sedangkan lintasan anabolisme merupakan lintasan yang bercabang keluar dari lintasan ini dengan penyediaan substrat senyawa karbon untuk keperluan biosintesis.
Metabolom dan jenjang reaksi pada siklus ini merupakan hasil karya Albert Szent-Györgyi and Hans Krebs.
Pada sel eukariota, siklus asam sitrat terjadi pada mitokondria, sedangkan pada organisme aerob, siklus ini merupakan bagian dari lintasan metabolisme yang berperan dalam konversi kimiawi terhadap karbohidrat, lemak dan protein - menjadi karbon dioksida, air, dalam rangka menghasilkan suatu bentuk energi yang dapat digunakan. Reaksi lain pada lintasan katabolisme yang sama, antara lain glikolisis, oksidasi asam piruvat dan fosforilasi oksidatif.
Produk dari siklus asam sitrat adalah prekursor bagi berbagai jenis senyawa organik. Asam sitrat merupakan prekursor dari kolesterol dan asam lemak, asam ketoglutarat-alfa merupakan prekursor dari asam glutamat, purina dan beberapa asam amino, suksinil-KoA merupakan prekursor dari heme dan klorofil, asam oksaloasetat merupakan prekursor dari asam aspartat, purina, pirimidina dan beberapa asam amino.[3]
Sekilas proses
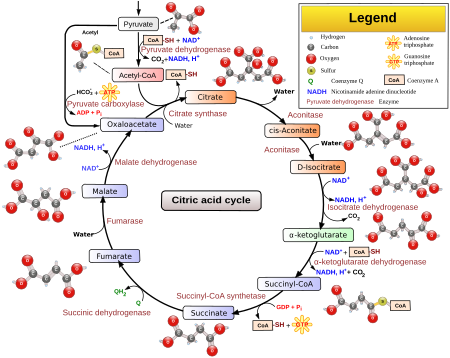
Siklus asam sitrat dimulai dengan satu molekul asetil-KoA bereaksi dengan satu molekul H2O, melepaskan gugus koenzim-A, dan mendonorkan dua atom karbon yang tersisa dalam bentuk gugus asetil kepada asam oksaloasetat yang memiliki molekul dengan empat atom karbon, hingga menghasilkan asam sitrat dengan enam atom karbon.[4][5]
| Substrat | Produk | Enzim | Reaksi | Keterangan | |
|---|---|---|---|---|---|
| 1 | Oksaloasetat + Asetil-KoA |
Asam sitrat + CoA-SH + H+ |
Sitrat sintase | Hidrolisis | Setelah enzim sitrat sintase melepaskan satu ion H+ dari molekul CH3 gugus asetil dari asetil-KoA, molekul CH2- pada gugus asetil tersebut akan bereaksi dengan asam oksaloasetat membentuk metabolit S-sitril-KoA. Reaksi hidrolisis yang terjadi selanjutnya pada gugus koenzim-A akan mendorong reaksi hingga menghasilkan tiga jenis produk. |
| 2 | Asam sitratberada pada matriks mitokonria | cis-Asonitat + H2O |
Asonitase | Dehidrasi | Reaksi isomerisasi terjadi dengan dua tahap, enzim asonitase akan melepaskan gugus air dari asam sitrat membentuk metabolit cis-Asonitat, kemudian terjadi penambahan kembali molekul air dengan pergeseran lokasi gugus hidroksil dan menghasilkan isomer asam sitrat. |
| 3 | cis-Asonitat + H2O |
Isositrat | Hidrasi | ||
| 4 | Isositrat + NAD+ |
Oksalosuksinat + NADH + H + |
Isositrat dehidrogenase | Oksidasi | Enzim isositrat dehidrogenase bersama dengan koenzim NAD+ akan mengubah gugus karboksil menjadi gugus karbonil, membentuk senyawa intermediat yang disebut oksalosuksinat. Eksitasi oleh ion H+ akan menyebabkan oksalosuksinat melepaskan gugus COO- yang tidak stabil dan membentuk senyawa CO2. |
| 5 | Oksalosuksinat | Ketoglutarat-α + CO2 |
Dekarboksilasi | ||
| 6 | Ketoglutarat-α + NAD+ + CoA-SH |
Suksinil-KoA + NADH + H+ + CO2 |
Ketoglutarat-α dehidrogenase | Dekarboksilasi | Kompleks dehidrogenase ketoglutarat-alfa mirip kompleks piruvat dehidrogenase yang menjadi enzim pada transformasi asam piruvat menjadi asetil-KoA. Bersama dengan koenzim NAD+ akan mempercepat oksidasi yang membentuk koenzim baru, disebut suksinil-KoA, yang memiliki ikatan tioester antara koenzim-A dengan gugus suksinil. |
| 7 | Suksinil-KoA + GDP + Pi + H2O |
Suksinat + CoA-SH + GTP |
Suksinil-KoA sintetase | fosforilasi substrat | Senyawa Pi akan menggantikan gugus CoA pada suksinat, kemudian didonorkan ke GDP untuk membentuk GTP. Pada bakteri dan tumbuhan, gugus Pi akan didonorkan ke ADP guna menghasilkan ATP. |
| 8 | Suksinat + FAD |
Fumarat + FADH2 |
Suksinat dehidrogenase | Oksidasi | |
| 9 | Fumarat + H2O |
Malat | Fumarase | Hidrasi | Reaksi penambahan molekul air pada fumarat akan menjadi gugus hidroksil pada senyawa baru. |
| 10 | Malat + NAD+ |
Oksaloasetat + NADH + H+ |
Malat dehidrogenase | Oksidasi | Reaksi oksidasi yang terakhir akan mengubah gugus hidroksil menjadi karbonil dan menghasilkan senyawa pertama siklus sitrat, yaitu asam oksaloasetat. |
Lihat pula
Rujukan
- ^ (Inggris)Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter (2002). Molecular Biology of the Cell - How Cells Obtain Energy from Food (edisi ke-4). Garland Science. ISBN 0-8153-3218-1. Diakses tanggal 2010-07-11.
- ^ (Inggris)Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter (2002). Molecular Biology of the Cell - How Cells Obtain Energy from Food : Fig. 2-88. Glycolysis and the citric acid cycle are at the center of metabolism (edisi ke-4). Garland Science. ISBN 0-8153-3218-1. Diakses tanggal 2010-07-16.
- ^ (Inggris)Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter (2002). Molecular Biology of the Cell - Fig. 2-87. Glycolysis and the citric acid cycle provide the precursors needed to synthesize many important biological molecules (edisi ke-4). Garland Science. ISBN 0-8153-3218-1. Diakses tanggal 2010-07-16.
- ^ (Inggris)Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter (2002). Molecular Biology of the Cell - Simple overview of the citric acid cycle (edisi ke-4). Garland Science. ISBN 0-8153-3218-1. Diakses tanggal 2010-07-11.
- ^ (Inggris)Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter (2002). Molecular Biology of the Cell - Panel 2-9 The Complete Citric Acid Cycle (edisi ke-4). Garland Science. ISBN 0-8153-3218-1. Diakses tanggal 2010-07-14.