Amonium nitrat
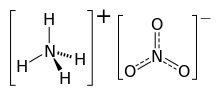
Amonium nitrat adalah suatu senyawa kimia, yang merupakan garam nitrat dari kation amonium. Senyawa ini memiliki rumus kimia NH4NO3, disederhanakan menjadi N2H4O3. Senyawa ini adalah padatan kristal putih dan sangat larut dalam air. Senyawa ini utamanya digunakan dalam pertanian sebagai pupuk kaya-nitrogen.[4] Penggunaan utama lainnya adalah sebagai komponen campuran peledak yang digunakan dalam konstruksi pertambangan, penggalian, dan konstruksi sipil. Senyawa ini adalah penyusun utama ANFO, sebuah industri peledak populer yang menyumbang 80% bahan peledak yang digunakan di Amerika Utara; formulasi serupa telah digunakan dalam alat peledak terimprovisasi. Banyak negara menghapusnya dalam aplikasi konsumen karena kekhawatiran akan potensi penyalahgunaannya.
| |

| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Amonium nitrat
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
| Nomor RTECS | {{{value}}} |
| UNII | |
| Nomor UN | 0222 – dengan > 0.2% zat terbakar 1942 – with <= 0.2% combustible substances 2067 – fertilizers 2426 – liquid |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| NH4NO3 | |
| Massa molar | 80.043 g/mol |
| Penampilan | padatan putih/abu |
| Densitas | 1.725 g/cm3 (20 °C) |
| Titik lebur | 169.6 °C |
| Titik didih | kira-kira 210 °C; terurai |
| 118 g/100 ml (0 °C) 150 g/100 ml (20 °C) 297 g/100 ml (40 °C) 410 g/100 ml (60 °C) 576 g/100 ml (80 °C) 1024 g/100 ml (100 °C)[1] | |
| -33.6·10−6 cm3/mol | |
| Struktur | |
| trigonal | |
| Data eksplosif | |
| Sensitivitas goncangan | sangat rendah |
| Sensitivitas gesekan | sangat rendah |
| Kecepatan ledakan | 5270 m/s |
| Bahaya | |
| Bahaya utama | Explosive |
| Lembar data keselamatan | ICSC 0216 |
Klasifikasi UE (DSD) (usang)
|
|
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
2085–5300 mg/kg (oral dalam tikus)[2] |
| Senyawa terkait | |
Anion lain
|
Amonium nitrit |
Kation lainnya
|
Natrium nitrat Kalium nitrat Hidroksilamonium nitrat |
Senyawa terkait
|
Amonium perklorat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Keberadaan
suntingAmonium nitrat ditemukan sebagai mineral alami (amonia nitre—analog amonium garam dan mineral nitre lainnya seperti natrium nitrat) di daerah paling kering di Gurun Atacama di Chile, sering Sebagai kerak di tanah dan/atau bersamaan dengan nitrat lainnya, klorat, iodat, dan mineral halida. Amonium nitrat ditambang di sana di masa lalu, namun hampir 100% bahan kimia yang saat ini digunakan adalah sintetik.
Produksi
suntingProduksi industri amonium nitrat mengandung asam basa amonia dengan asam nitrat:[5]
- HNO3 + NH3 → NH4NO3
Amonia digunakan dalam bentuk anhidratnya (yaitu bentuk gas) dan asam nitrat terkonsentrasi. Reaksi ini berlangsung keras karena sifatnya yang sangat eksotermik. Setelah larutan terbentuk, biasanya pada konsentrasi sekitar 83%, kelebihan air diuapkan menjadi kandungan amonium nitrat (AN) sebesar 95% sampai konsentrasi 99,9% (AN meleleh), tergantung pada kadarnya. Lelehan AN kemudian dibuat menjadi "prills" atau manik-manik kecil dalam menara semprot, atau menjadi butiran dengan menyemprotkannya dan berjatuhan di drum yang berputar. Potongan atau butiran tersebut dapat dikeringkan lebih lanjut, didinginkan, lalu dilapisi untuk mencegah pengeringan. Potongan atau butiran ini adalah produk AN yang khas dalam perdagangan.
Amonia yang dibutuhkan untuk proses ini diperoleh dengan proses Haber dari nitrogen dan hidrogen. Amonia yang dihasilkan oleh proses Haber dioksidasi menjadi asam nitrat oleh proses Ostwald. Metode produksi lain adalah varian dari proses Odda:
Produknya, kalsium karbonat dan amonium nitrat, dapat secara terpisah dimurnikan atau dijuan tergabung sebagai kalsium amonium nitrat.
Amonium nitrat dapat pula dibuat melalui reaksi metatesis:
Reaksi
suntingAmonium nitrat bereaksi dengan logam hidroksida, melepaskan amonia dan membentuk alkali logam nitrat:
- NH4NO3 + MOH → NH3 + H2O + MNO3 (M = Na, K)
Amonium nitrat tidak meninggalkan residu ketika dipanaskan:
- NH4NO3 → N2O + 2H2O
Amonium nitrat juga terbentuk dalam atmosfer Bumi dari emisi NO, SO2, dan NH3, dan merupakan komponen sekunder dari PM10.[6]
Bencana
suntingAmonium nitrat terurai menjadi gas dinitrogen oksida dan uap air bila dipanaskan (bukan reaksi eksplosif); namun, dapat diinduksi untuk meluruh secara eksplosif oleh ledakan. Stok bahan yang besar bisa menjadi risiko kebakaran utama karena oksidasi pendukungnya, dan mungkin juga meledak, seperti yang terjadi pada bencana di Texas City pada tahun 1947, yang menyebabkan perubahan besar dalam peraturan untuk penyimpanan dan penanganannya.
Dua kelas utama insiden yang mengakibatkan ledakan adalah:
- Ledakan terjadi oleh mekanisme transisi shock-to-detonation. Inisiasi terjadi dengan muatan peledak yang meledak dalam massa, dengan peledakan tempurung yang dilemparkan ke dalam massa, atau dengan meledakkan campuran peledak yang kontak dengan massa tersebut. Contohnya adalah Kriewald, Morgan (saat ini Sayreville, New Jersey), Oppau, dan Tessenderlo.
- Ledakan yang berasal dari api yang menyebar ke amonium nitrat itu sendiri (Texas City, Brest, Oakdale PA), atau dari campuran amonium nitrat dengan bahan yang mudah terbakar selama kebakaran (Repauno, Cherokee, Nadadores). Api harus dibatasi setidaknya sampai tingkat tertentu untuk transisi yang berhasil dari api ke sebuah ledakan (sebuah fenomena yang dikenal sebagai "transisi deflagration-to-detonation"). AN murni, yang kompak bersifat stabil dan sangat sulit untuk menyala, dan banyak kasus hadir bahkan bila AN yang tidak murni tidak meledak dalam api.
Referensi
sunting- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ Martel, B.; Cassidy, K. (2004). Chemical Risk Analysis: A Practical Handbook. Butterworth–Heinemann. hlm. 362. ISBN 1-903996-65-1.
- ^ "Archived copy". Diarsipkan dari versi asli tanggal 2015-02-17. Diakses tanggal 2015-03-13.
- ^ Karl-Heinz Zapp "Ammonium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry 2012, Wiley-VCH, Weinheim. doi:10.1002/14356007.a02_243
- ^ http://www.google.com/patents/pdf/Process_of_producing_concentrated_soluti.pdf?id=XronAAAAEBAJ&output=pdf&sig=ACfU3U0iYFRDUxltKLaVind-3wwP_JYPxg
- ^ Int Panis, LLR (2008). "The Effect of Changing Background Emissions on External Cost Estimates for Secondary Particulates" (PDF). Open Environmental Sciences. 2: 47–53. doi:10.2174/1876325100802010047.[pranala nonaktif permanen]
- Properties: UNIDO and International Fertilizer Development Center (1998), Fertilizer Manual, Kluwer Academic Publishers, ISBN 0-7923-5032-4.
Pranala luar
sunting- International Chemical Safety Card 0216
- "Storing and Handling Ammonium Nitrate", United Kingdom Health and Safety Executive publication INDG230 (1986)
- Chemical Advisory: Safe Storage, Handling, and Management of Ammonium Nitrate United States Environmental Protection Agency
- Kalkulator: Tegangan permukaan, dan densitas, molaritas dan molalitas dari larutan amonium nitrat
| HNO3 | He | ||||||||||||||||||
| LiNO3 | Be(NO''"; | B(NO''"; | C | N | O | FNO3 | Ne | ||||||||||||
| NaNO3 | Mg(NO''"; | Al(NO''"; | Si | P | S | ClONO2 | Ar | ||||||||||||
| KNO3 | Ca(NO''"; | Sc(NO''"; | Ti(NO''"; | VO(NO''"; | Cr(NO''"; | Mn(NO''"; | Fe(NO''"; | Co(NO''";, Co(NO''"; |
Ni(NO''"; | Cu(NO''"; | Zn(NO''"; | Ga(NO''"; | Ge | As | Se | Br | Kr | ||
| RbNO | Sr(NO''"; | Y | Zr(NO''"; | Nb | Mo | Tc | Ru | Rh | Pd(NO''"; | AgNO | Cd(NO''"; | In | Sn | Sb | Te | I | Xe(NO''"; | ||
| CsNO | Ba(NO''"; | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg, Hg(NO''"; |
Tl(NO''"; | Pb(NO''"; | Bi(NO''"; | Po | At | Rn | |||
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Fl | Uup | Lv | Uus | Uuo | |||
| ↓ | |||||||||||||||||||
| La | Ce(NO''";, Ce(NO''"; |
Pr | Nd | Pm | Sm | Eu | Gd(NO''"; | Tb | Dy | Ho | Er | Tm | Yb | Lu | |||||
| Ac | Th | Pa | UO | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | |||||