Skandium klorida
Skandium(III) klorida adalah senyawa anorganik dengan rumus ScCl3. Ini adalah senyawa ionik putih yang mudah meleleh, yang bersifat sangat larut dalam air. [2] Garam ini terutama diminati di laboratorium penelitian. Baik bentuk anhidrat maupun heksahidrat (ScCl3•6H2O) tersedia secara komersial.
| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Scandium(III) klorida
| |
| Nama lain
skandium klorida
skandium triklorida | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| ScCl3 | |
| Massa molar | 151.31 g/mol |
| Penampilan | kristal putih keabu-abuan |
| Densitas | 2.39 g/mL, padat |
| Titik lebur | 960 °C (1.760 °F; 1.230 K)[1] 63 °C (heksahidrat) |
| larut | |
| Kelarutan dalam pelarut lain | tidak larut dalam EtOH |
| Bahaya | |
| Bahaya utama | Iritan |
| Lembar data keselamatan | External MSDS |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
3980 mg/kg (tikus, oral) |
| Senyawa terkait | |
Anion lain
|
Skandium(III) fluorida Skandium bromida Skandium triiodida |
Kation lainnya
|
Itrium(III) klorida Lutesium(III) klorida |
Senyawa terkait
|
Skandium(III) nitrat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Struktur
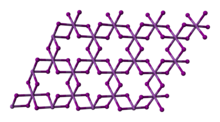
ScCl3 mengkristal dalam motif BiI3 berlapis, yang menonjolkan pusat skandium oktahedral.[3] Monomer ScCl3 adalah spesi dominan dalam fase uap pada 900 K, dimer Sc2Cl6 menyumbang sekitar 8%.[4] Spektrum difraksi elektron menunjukkan bahwa monomer adalah planar dan dimer memiliki dua penghubung atom Cl masing-masing Sc menjadi 4 koordinat.[4]
Reaksi
ScCl3 adalah asam Lewis yang menyerap air untuk menghasilkan kompleks aquo. Berdasarkan kristalografi sinar-X, salah satu hidrat tersebut adalah garam trans-[ScCl2(H2O)4]Cl·2H2O.[5] Dengan ligan yang kurang basa tetrahidrofuran, ScCl3 menghasilkan campuran ScCl3(TH)3 sebagai kristal putih. Kompleks yang larut dalam THF ini digunakan dalam sintesis senyawa organoskandium.[6] ScCl3 telah diubah menjadi garam dodesil sulfatnya, yang telah diselidiki sebagai "katalis gabungan surfaktan asam Lewis" (LASC) dalam reaksi mirip aldol.[7]
Reduksi
Skandium(III) klorida digunakan oleh Karl Fischer yang pertama kali membuat skandium logam dengan elektrolisis lelehan eutektik skandium(III) klorida dan garam lainnya pada 700-800 °C.[8]
ScCl3 bereaksi dengan logam skandium menghasilkan sejumlah klorida dimana skandium memiliki bilangan oksidasi <+3, ScCl, Sc7Cl10, Sc2Cl3, Sc5Cl8 dan Sc7Cl12.[2][9] Sebagai contoh, reduksi ScCl3 dengan logam skandium dengan adanya sesium klorida menghasilkan senyawa CsScCl3 yang mengandung rantai linier komposisi ScIICl3−, mengandung ScIICl6 oktahedra berbagi muka.[10]
Penggunaan
Skandium(III) klorida ditemukan di beberapa lampu halida, serat optik, keramik elektronik, dan laser.[11]
Referensi
- ^ Frederikse, H.P.R.; Lide, David R. (1998). CRC Handbook of Chemistry and Physics (78th Edition)
- ^ a b Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- ^ Crystal Structure of ScCl3 Refined from Powder Neutron Diffraction Data, Fjellvåg, H., Karen, P., Acta Chemica Scandinavica, 48, 294-297, DOI:10.3891/acta.chem.scand.48-0294
- ^ a b Haaland A., Martinsen K-G, Shorokhov D.J, Girichev G.V., Sokolov V.I, J. Chem. Soc., Dalton Trans., 1998, 2787 - 2792, DOI:10.1039/a803339k
- ^ The Rare Earth Elements, Fundamentals and Applications David A. Atwood, 2012, John Wiley & Sons Inc, ISBN 9781119950974
- ^ Manzer, L. E., "Tetrahydrofuran Complexes of Selected Early Transition Metals", Inorganic Syntheses, 1982, volume 21, page 135-40.DOI:10.1002/9780470132524.ch31
- ^ Manabe, Kei; Mori, Yuichiro; Kobayashi, Shū (1999). "Effects of Lewis acid-surfactant-combined catalysts on aldol and Diels-Alder reactions in water". Tetrahedron. 55 (37): 11203–11208. doi:10.1016/S0040-4020(99)00642-0.
- ^ Fischer, Werner; Brünger, Karl; Grieneisen, Hans (1937). "Über das metallische Scandium". Zeitschrift für anorganische und allgemeine Chemie. 231 (1–2): 54–62. doi:10.1002/zaac.19372310107.
- ^ Corbett, J.D. (1981). "Extended metal-metal bonding in halides of the early transition metals". Acc. Chem. Res. 14 (8): 239–246. doi:10.1021/ar00068a003.
- ^ Meyer, Gerd.; Corbett, John D. (1981). "Reduced ternary halides of scandium: RbScX3 (X = chlorine, bromine) and CsScX3 (X = chlorine, bromine, iodine)". Inorganic Chemistry. 20 (8): 2627–2631. doi:10.1021/ic50222a047. ISSN 0020-1669.
- ^ Metal Suppliers Online. (2000). Scandium Chloride