Apigenin
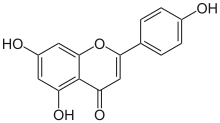
Apigenin (4′,5,7-trihidroksiflavon), yang ditemukan di banyak tanaman, adalah produk alami yang termasuk dalam golongan flavon yang merupakan aglikon dari beberapa glikosida yang terdapat di alam. Produk ini berupa padatan kristal berwarna kuning yang telah digunakan untuk mewarnai wol.
| |

| |
| Nama | |
|---|---|
| Nama IUPAC
4′,5,7-Trihidroksiflavon
| |
| Nama IUPAC (sistematis)
5,7-Dihidroksi-2-(4-hidroksifenil)-4H-1-benzopiran-4-ona | |
| Nama lain
Kamomil; Apigenol; Spigenin; Versulin; C.I. Natural Yellow 1
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Nomor EC | |
| KEGG | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C15H10O5 | |
| Massa molar | 270,24 g·mol−1 |
| Penampilan | Padatan kristal berwarna kuning |
| Titik lebur | 345–350 °C (653–662 °F; 618–623 K) |
| λmaks | 267, 296sh, 336 nm pada metanol[2] |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Sumber di alam
suntingApigenin ditemukan dalam banyak buah-buahan dan sayuran; tetapi peterseli, seledri, dan teh kamomil adalah sumber yang paling umum.[3] Apigenin sangat melimpah di bunga tanaman kamomil, yang merupakan 68% dari total flavonoid.[4] Peterseli kering dapat mengandung sekitar 45 mg apigenin/gram herba, dan bunga kamomil kering sekitar 3–5 mg/gram.[5] Kandungan apigenin peterseli segar dilaporkan 215,5 mg/100 gram, yang jauh lebih tinggi dari sumber makanan tertinggi berikutnya, yakni jantung seledri hijau yang menyediakan 19,1 mg/100 gram apigenin.[6]
Farmakologi
suntingApigenin secara kompetitif mengikat situs benzodiazepin pada reseptor GABAA.[7] Ada temuan yang bertentangan mengenai bagaimana apigenin berinteraksi dengan situs ini.[8][9] Apigenin dapat meningkatkan aktivitas enzim antioksidan endogen seperti SOD dan CAT, membantu mengurangi stres oksidatif.[10][11]
Biosintesis
suntingApigenin secara biosintesis berasal dari jalur fenilpropanoid umum dan jalur sintesis flavon.[12] Jalur fenilpropanoid dimulai dari asam amino aromatik L-fenilalanina atau L-tirosina, keduanya merupakan produk dari jalur sikimat.[13] Ketika dimulai dari L-fenilalanina, pertama-tama asam amino tersebut dideaminasi secara non-oksidatif oleh fenilalanina amonia liase (PAL) untuk menghasilkan sinamat, diikuti oleh oksidasi pada posisi para oleh sinamat 4-hidroksilase (C4H) untuk menghasilkan p-kumarat. Karena L-tirosin telah dioksidasi pada posisi para, ia melewati oksidasi ini dan hanya dideaminasi oleh tirosin amonia liase (TAL) untuk menghasilkan p-kumarat.[14] Untuk melengkapi jalur fenilpropanoid umum, 4-kumarat CoA ligase (4CL) menggantikan koenzim A (CoA) pada gugus karboksi p-kumarat. Memasuki jalur sintesis flavon, enzim sintase poliketida tipe III kalkon sintase (CHS) menggunakan kondensasi berurutan dari tiga ekuivalen malonil-KoA diikuti oleh aromatisasi untuk mengubah p-kumaroil-CoA menjadi kalkon.[15] Kalkon isomerase (CHI) kemudian mengisomerisasi produk untuk menutup cincin piron untuk membuat naringenin. Akhirnya, enzim sintase flavanon (FNS) mengoksidasi naringenin menjadi apigenin.[16] Dua jenis FNS telah dijelaskan sebelumnya; FNS I, enzim larut yang menggunakan 2-oksogluturat, Fe2+, dan askorbat sebagai kofaktor dan FNS II, monooksigenase sitokrom p450 yang terikat membran dan bergantung NADPH.[17]
Glikosida
suntingGlikosida alami yang terbentuk dari kombinasi apigenin dengan gula meliputi:
- Apiin (apigenin 7-O-apioglukosida), diisolasi dari peterseli[18] dan seledri
- Apigetrin (apigenin 7-glukosida), ditemukan dalam kopi dandelion
- Viteksin (apigenin 8-C-glukosida)
- Isoviteksin (apigenin 6-C-glukosida)
- Roifolin (apigenin 7-O-neohesperidosida)
- Skaftosida (apigenin 6-C-glukosida 8-C-arabinosida)
Dalam diet
suntingBeberapa makanan mengandung apigenin dalam jumlah yang relatif tinggi:[19]
| Produk | Apigenin (miligram per 100 gram) |
|---|---|
| Peterseli kering | 4500[5] |
| Kamomil | 300–500 |
| Peterseli | 215,5 |
| Jantung seledri, hijau | 19,1 |
| Rutabaga mentah | 4 |
Referensi
sunting- ^ Merck Index, 11th Edition, 763.
- ^ The Systematic Identification of Flavonoids. Mabry et al, 1970, page 81
- ^ The compound in the Mediterranean diet that makes cancer cells 'mortal' Emily Caldwell, Medical Express, May 20, 2013.
- ^ Venigalla M, Gyengesi E, Münch G (August 2015). "Curcumin and Apigenin – novel and promising therapeutics against chronic neuroinflammation in Alzheimer's disease". Neural Regeneration Research. 10 (8): 1181–5. doi:10.4103/1673-5374.162686 . PMC 4590215 . PMID 26487830.
- ^ a b Shankar E, Goel A, Gupta K, Gupta S (2017). "Plant flavone apigenin: An emerging anticancer agent". Current Pharmacology Reports. 3 (6): 423–446. doi:10.1007/s40495-017-0113-2. PMC 5791748 . PMID 29399439.
- ^ Delage, PhD, Barbara (November 2015). "Flavonoids". Corvallis, Oregon: Linus Pauling Institute, Oregon State University. Diakses tanggal 2021-01-26.
- ^ Viola, H.; Wasowski, C.; Levi de Stein, M.; Wolfman, C.; Silveira, R.; Dajas, F.; Medina, J. H.; Paladini, A. C. (June 1995). "Apigenin, a component of Matricaria recutita flowers, is a central benzodiazepine receptors-ligand with anxiolytic effects". Planta Medica. 61 (3): 213–216. doi:10.1055/s-2006-958058. ISSN 0032-0943. PMID 7617761.
- ^ Dekermendjian, K.; Kahnberg, P.; Witt, M. R.; Sterner, O.; Nielsen, M.; Liljefors, T. (1999-10-21). "Structure-activity relationships and molecular modeling analysis of flavonoids binding to the benzodiazepine site of the rat brain GABA(A) receptor complex". Journal of Medicinal Chemistry. 42 (21): 4343–4350. doi:10.1021/jm991010h. ISSN 0022-2623. PMID 10543878.
- ^ Avallone, R.; Zanoli, P.; Puia, G.; Kleinschnitz, M.; Schreier, P.; Baraldi, M. (2000-06-01). "Pharmacological profile of apigenin, a flavonoid isolated from Matricaria chamomilla". Biochemical Pharmacology. 59 (11): 1387–1394. doi:10.1016/s0006-2952(00)00264-1. ISSN 0006-2952. PMID 10751547.
- ^ Blanca (Aug 7, 2024). "Top 6 Benefits of Apigenin for Health". Stanford Chemicals. Diakses tanggal Oct 16, 2024.
- ^ Singh, Abhinav; Singh, Jagjit (2024). "A comprehensive review of apigenin a dietary flavonoid: biological sources, nutraceutical prospects, chemistry and pharmacological insights and health benefits". Critical Reviews in Food Science and Nutrition: 1–37. doi:10.1080/10408398.2024.2390550. PMID 39154213 Periksa nilai
|pmid=(bantuan). - ^ Forkmann, G. (January 1991). "Flavonoids as Flower Pigments: The Formation of the Natural Spectrum and its Extension by Genetic Engineering". Plant Breeding (dalam bahasa Inggris). 106 (1): 1–26. doi:10.1111/j.1439-0523.1991.tb00474.x . ISSN 0179-9541.
- ^ Herrmann KM (January 1995). "The shikimate pathway as an entry to aromatic secondary metabolism". Plant Physiology. 107 (1): 7–12. doi:10.1104/pp.107.1.7. PMC 161158 . PMID 7870841.
- ^ Lee H, Kim BG, Kim M, Ahn JH (September 2015). "Biosynthesis of Two Flavones, Apigenin and Genkwanin, in Escherichia coli". Journal of Microbiology and Biotechnology. 25 (9): 1442–8. doi:10.4014/jmb.1503.03011 . PMID 25975614.
- ^ Austin MB, Noel JP (February 2003). "The chalcone synthase superfamily of type III polyketide synthases". Natural Product Reports. 20 (1): 79–110. CiteSeerX 10.1.1.131.8158 . doi:10.1039/b100917f. PMID 12636085.
- ^ Martens S, Forkmann G, Matern U, Lukacin R (September 2001). "Cloning of parsley flavone synthase I". Phytochemistry. 58 (1): 43–6. Bibcode:2001PChem..58...43M. doi:10.1016/S0031-9422(01)00191-1. PMID 11524111.
- ^ Leonard E, Yan Y, Lim KH, Koffas MA (December 2005). "Investigation of two distinct flavone synthases for plant-specific flavone biosynthesis in Saccharomyces cerevisiae". Applied and Environmental Microbiology. 71 (12): 8241–8. Bibcode:2005ApEnM..71.8241L. doi:10.1128/AEM.71.12.8241-8248.2005. PMC 1317445 . PMID 16332809.
- ^ Meyer H, Bolarinwa A, Wolfram G, Linseisen J (2006). "Bioavailability of apigenin from apiin-rich parsley in humans". Annals of Nutrition & Metabolism. 50 (3): 167–72. doi:10.1159/000090736. PMID 16407641.
- ^ USDA Database for the Flavonoid Content of Selected Foods, Release 3 (2011)