Apiksaban
Apiksaban adalah obat antikoagulan yang digunakan untuk mengobati dan mencegah pembekuan darah serta mencegah strok pada orang dengan fibrilasi atrium nonvalvular melalui penghambatan faktor Xa secara langsung.[1][2][3] Obat ini digunakan sebagai alternatif warfarin untuk mencegah pembekuan darah setelah penggantian pinggul atau lutut dan pada mereka yang memiliki riwayat pembekuan darah sebelumnya.[1][3] dan tidak memerlukan pemantauan dengan tes darah[1] atau pembatasan diet.[4] Obat ini digunakan dengan cara diminum.[1]
| |
|---|---|

| |
| Nama sistematis (IUPAC) | |
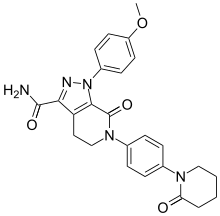
| 1-(4-metoksifenil)-7-okso-6-[4-(2-oksopiperidin-1-il)fenil]-4,5,6,7-tetrahidro-1H-pirazolo[3,4-c]piridina-3-karboksamida | |
| Data klinis | |
| Nama dagang | Eliquis, dll |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a613032 |
| Data lisensi | US Daily Med:pranala |
| Kat. kehamilan | C(AU) |
| Status hukum | POM (UK) ℞-only (US) ℞ Preskripsi saja |
| Rute | Oral |
| Data farmakokinetik | |
| Bioavailabilitas | ~50% |
| Ikatan protein | ~87% |
| Metabolisme | CYP3A4, CYP3A5, CYP1A2 dan lainnya |
| Waktu paruh | 9–14 jam |
| Ekskresi | Saluran empedu (75%), ginjal (25%) |
| Pengenal | |
| Nomor CAS | 503612-47-3 |
| Kode ATC | B01AF02 |
| PubChem | CID 10182969 |
| Ligan IUPHAR | 6390 |
| DrugBank | DB07828 |
| ChemSpider | 8358471 |
| UNII | 3Z9Y7UWC1J |
| KEGG | D03213 |
| ChEMBL | CHEMBL231779 |
| Sinonim | BMS-562247-01 |
| Data kimia | |
| Rumus | C25H25N5O4 |
| |
Efek samping yang umum termasuk [[perdarahan][ dan mual.[1][2] Efek samping lainnya mungkin termasuk pendarahan di sekitar tulang belakang dan reaksi alergi.[1] Penggunaan obat ini tidak dianjurkan selama kehamilan atau menyusui.[5][2] Penggunaan obat ini tampaknya relatif aman pada mereka yang memiliki masalah ginjal ringan.[2] Dibandingkan dengan warfarin, obat ini memiliki lebih sedikit interaksi dengan obat lain.[6] Obat ini merupakan penghambat faktor Xa secara langsung.[1]
Pada tahun 2007, Pfizer dan Bristol Myers Squibb mulai mengembangkan apiksaban sebagai antikoagulan.[7] Apiksaban disetujui untuk penggunaan medis di Uni Eropa pada bulan Mei 2011, dan di Amerika Serikat pada bulan Desember 2012.[8][1][9] Obat ini masuk dalam Daftar Obat Esensial Organisasi Kesehatan Dunia.[10] Obat ini tersedia sebagai obat generik. Obat ini tidak tersedia di Amerika Serikat.[3][11]
Sejarah
suntingApiksaban disetujui untuk penggunaan medis di Uni Eropa pada bulan Mei 2011.[8]
Aplikasi obat baru (NDA) untuk persetujuan apiksaban diajukan ke Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) oleh Bristol-Myers Squibb (BMS) dan Pfizer bersama-sama setelah uji klinis ARISTOTLE selesai pada tahun 2011.[12][9] Apiksaban disetujui untuk pencegahan strok pada orang dengan fibrilasi atrium pada bulan Desember 2012.[9][13] Pada bulan Maret 2014, obat ini disetujui untuk indikasi tambahan pencegahan trombosis vena dalam dan emboli paru pada orang yang baru saja menjalani penggantian lutut atau pinggul.[14][15] Pada bulan Agustus 2014, FDA menyetujui apiksaban untuk indikasi tambahan pengobatan trombosis vena dalam dan emboli paru yang berulang.[14][16] Selama pengembangannya, obat ini dikenal sebagai BMS-562247-01.[17] Pada akhir tahun 2019, penjualan produk BMS mencapai tiga puluh persen dari pendapatan kuartalan mereka.[18]
Kegunaan dalam medis
suntingApiksaban diindikasikan untuk hal-hal berikut:[19]
- Untuk menurunkan risiko stroke dan embolisme pada orang dengan fibrilasi atrium nonvalvular.
- Pencegahan trombosis vena dalam (DVT). DVT dapat menyebabkan emboli paru (PE) pada pasien operasi penggantian lutut atau pinggul.
- Pengobatan DVT dan PE.
- Untuk mengurangi risiko DVT dan PE berulang setelah terapi awal.
Di UE, apiksaban diindikasikan untuk pencegahan kejadian tromboemboli vena (VTE) pada orang dewasa yang telah menjalani operasi penggantian pinggul atau lutut elektif, pencegahan strok dan emboli sistemik pada orang dewasa dengan fibrilasi atrium nonvalvular (NVAF) dengan satu atau lebih faktor risiko, untuk pengobatan trombosis vena dalam (DVT) dan emboli paru (PE) pada orang dewasa, dan untuk pencegahan DVT dan PE berulang pada orang dewasa.[8]
Fibrilasi atrium
suntingApiksaban direkomendasikan oleh National Institute for Health and Clinical Excellence untuk pencegahan stroke dan emboli sistemik pada orang dengan fibrilasi atrium non-katup dan setidaknya satu dari faktor risiko berikut: riwayat strok atau serangan iskemik transien, usia 75 tahun atau lebih, diabetes melitus, atau gagal jantung simptomatik.[20]
Apiksaban dan antikoagulan lainnya (dabigatran, edoksaban, dan rivaroksaban) tampaknya sama efektifnya dengan warfarin dalam mencegah strok non-hemoragik pada orang dengan fibrilasi atrium dan dikaitkan dengan risiko perdarahan intrakranial yang lebih rendah.[21][22]
Meskipun apiksaban dapat digunakan pada orang dengan fungsi ginjal yang sangat menurun dan mereka yang menjalani hemodialisis, namun belum diteliti pada kelompok ini.[1]
Efek samping
suntingPerdarahan
suntingApixaban dapat meningkatkan risiko perdarahan yang dapat serius dan berpotensi fatal. Penggunaan bersamaan dengan obat lain yang memengaruhi pembekuan darah dapat semakin meningkatkan risiko ini. Efek samping ini juga ditimbulkan oleh obat-obatan seperti antikoagulan lain, heparin, aspirin, obat antiplatelet, penghambat penyerapan kembali serotonin selektif, penghambat penyerapan kembali serotonin-norepinefrin, dan obat antiinflamasi nonsteroid (OAINS).[19][23][24][25]
Andeksanet alfa adalah antidot apiksaban yang disetujui Badan Pengawas Obat dan Makanan AS (FDA) pada orang dengan kejadian perdarahan yang tidak terkontrol dan mengancam jiwa.[26][27]
Tusukan tulang belakang
suntingSetelah anestesi atau tusukan tulang belakang, orang yang dirawat dengan agen antitrombotik berisiko lebih tinggi mengalami hematoma, yang menyebabkan kelumpuhan jangka panjang atau permanen. Risiko ini dapat meningkat dengan menggunakan kateter epidural atau intratekal setelah operasi bedah, atau dari penggunaan bersamaan agen obat yang memengaruhi hemostasis.[19]
Mekanisme kerja
suntingApiksaban adalah penghambat langsung faktor Xa bebas dan terikat bekuan darah yang sangat selektif, tersedia secara hayati secara oral, dan reversibel. Faktor Xa mengkatalisis konversi protrombin menjadi trombin, enzim terakhir dalam kaskade koagulasi yang bertanggung jawab atas pembentukan bekuan fibrin.[28] Apiksaban tidak memiliki efek langsung pada agregasi keping darah, tetapi dengan menghambat faktor Xa, secara tidak langsung menurunkan pembentukan bekuan darah yang disebabkan oleh trombin.[19]
Dalam budaya masyarakat
suntingEkonomi
suntingPada bulan Desember 2019, FDA menyetujui versi generik apiksaban yang diproduksi bersama oleh Mylan dan Micro Labs.[29][18][3] BMS dan Pfizer bekerja cepat untuk memblokir pembuatan obat generik, dan pada bulan Agustus 2020 mereka memenangkan gugatan pelanggaran paten terhadap Sigmapharm, Sunshine Lake, dan Unichem, setelah sebelumnya menyelesaikan kasus paten terhadap 25 perusahaan lain.[30][31] Pada bulan September 2021, Pengadilan Tinggi Federal Amerika Serikat untuk Wilayah Federal menguatkan putusan tersebut.[32] Hasilnya adalah obat generik apiksaban kemungkinan besar tidak akan tersedia di Amerika Serikat hingga setidaknya tahun 2026, tetapi mungkin tahun 2031.[11]
Pada bulan Juli 2022, perusahaan obat generik Kanada, Apotex Inc., memperoleh persetujuan untuk memasarkan apiksaban.[33][34]
Apiksaban adalah salah satu dari sepuluh obat yang dicakup oleh negosiasi harga di AS berdasarkan Undang-Undang Pengurangan Inflasi. Negosiasi yang dilakukan oleh Centers for Medicare & Medicaid Services berlaku untuk penetapan harga bagi penerima Medicare. Bristol Myers Squibb menanggapi laporan awal negosiasi tersebut dengan menyoroti harga langsung untuk Eliquis. Seorang eksekutif senior BMS berpendapat dalam wawancara pada bulan Agustus 2023 bahwa pasien sudah menerima harga langsung yang rendah, dengan berkomentar bahwa "para lansia rata-rata membayar sekitar [AS]$55 per bulan untuk Eliquis dan lebih dari setengah dari semua pasien Eliquis—baik pasien komersial maupun Medicare—membayar [AS]$45 atau kurang."[35] Hasil negosiasi diumumkan pada bulan Agustus 2024, dan harga yang dinegosiasikan Medicare untuk persediaan Eliquis selama 30 hari adalah US$231, turun 56% dari harga awal tahun 2023 sebesar US$521. Penetapan harga tersebut akan mulai berlaku pada tahun 2026.[36][37]
Referensi
sunting- ^ a b c d e f g h i "Apixaban Monograph for Professionals". Drugs.com. American Society of Health-System Pharmacists. Diakses tanggal 27 March 2019.
- ^ a b c d British national formulary: BNF 76 (edisi ke-76). Pharmaceutical Press. 2018. hlm. 124–125. ISBN 9780857113382.
- ^ a b c d "FDA approves first generics of Eliquis". U.S. Food and Drug Administration (FDA). 23 December 2019. Diarsipkan dari versi asli tanggal 23 December 2019. Diakses tanggal 23 December 2019. Artikel ini memuat teks dari sumber tersebut, yang berada dalam ranah publik.
- ^ Hall H (September–October 2020). "How a Drug Is Born". Skeptical Inquirer. Amherst, New York: Center for Inquiry.
- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamaDrugs.com pregnancy - ^ Kiser K (2017). Oral Anticoagulation Therapy: Cases and Clinical Correlation. Springer. hlm. 11. ISBN 9783319546438.
- ^ "Bristol-Myers Squibb and Pfizer Announce Worldwide Collaboration to Develop and Commercialize Anticoagulant and Metabolic Compounds". Pfizer (Siaran pers). Diarsipkan dari versi asli tanggal 10 September 2015. Diakses tanggal 25 December 2021.
- ^ a b c "Eliquis EPAR". European Medicines Agency. 17 September 2018. Diakses tanggal 22 April 2020. Text was copied from this source which is copyright European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ^ a b c "Drug Approval Package: Eliquis (apixaban) NDA #202155". U.S. Food and Drug Administration (FDA). 13 February 2013. Diakses tanggal 23 December 2019.
- ^ World Health Organization (2023). The selection and use of essential medicines 2023: web annex A: World Health Organization model list of essential medicines: 23rd list (2023). Geneva: World Health Organization. hdl:10665/371090 . WHO/MHP/HPS/EML/2023.02.
- ^ a b "With Court Win, BMS and Pfizer Stave Off Generic Challengers to Eliquis – For Now". BioSpace. 6 August 2020. Diakses tanggal 29 November 2021.
- ^ Granger CB, Alexander JH, McMurray JJ, Lopes RD, Hylek EM, Hanna M, Al-Khalidi HR, Ansell J, Atar D, Avezum A, Bahit MC, Diaz R, Easton JD, Ezekowitz JA, Flaker G, Garcia D, Geraldes M, Gersh BJ, Golitsyn S, Goto S, Hermosillo AG, Hohnloser SH, Horowitz J, Mohan P, Jansky P, Lewis BS, Lopez-Sendon JL, Pais P, Parkhomenko A, Verheugt FW, Zhu J, Wallentin L (September 2011). "Apixaban versus warfarin in patients with atrial fibrillation". The New England Journal of Medicine. 365 (11): 981–992. doi:10.1056/NEJMoa1107039 . PMID 21870978.
- ^ Cada DJ, Levien TL, Baker DE (June 2013). "Apixaban". Hospital Pharmacy. 48 (6): 494–509. doi:10.1310/hpj4806-494. PMC 3839491 . PMID 24421512.
- ^ a b "FDA-Approved Drugs: Eliquis (apixaban)". U.S. Food and Drug Administration (FDA). Diakses tanggal 23 December 2019.
- ^ Neale T (14 March 2014). "FDA OKs Apixaban for DVT Prevention". MedPage Today. Diakses tanggal 17 September 2015.
- ^ "U.S. FDA Approves Eliquis (apixaban) for the Treatment of Deep Vein Thrombosis (DVT) and Pulmonary Embolism (PE), and for the Reduction in the Risk of Recurrent DVT and PE Following Initial Therapy" (Siaran pers). Pfizer. 21 August 2014. Diakses tanggal 26 February 2016.
- ^ "Apixaban". PubChem, US National Library of Medicine. 27 August 2022. Diakses tanggal 2 September 2022.
- ^ a b "FIRST: Mylan, Micro Labs get USFDA nod for generic version of blood thinner Eliquis". Business Medical Dialogues. New Delhi, India: Minerva Medical Treatment. 24 December 2019. Diakses tanggal 24 December 2019.
- ^ a b c d "Eliquis- apixaban tablet, film coated Eliquis 30-day starter pack- apixaban kit". DailyMed. 26 November 2019. Diakses tanggal 22 April 2020.
- ^ "Apixaban for preventing stroke and systemic embolism in people with nonvalvular atrial fibrillation" (PDF). National Institute for Health and Care Excellence. January 2013. Diakses tanggal 26 February 2016.
- ^ Gómez-Outes A, Terleira-Fernández AI, Calvo-Rojas G, Suárez-Gea ML, Vargas-Castrillón E (2013). "Dabigatran, Rivaroxaban, or Apixaban versus Warfarin in Patients with Nonvalvular Atrial Fibrillation: A Systematic Review and Meta-Analysis of Subgroups". Thrombosis. 2013: 640723. doi:10.1155/2013/640723 . PMC 3885278 . PMID 24455237.
- ^ Lowenstern A, Al-Khatib SM, Sharan L, Chatterjee R, Allen LaPointe NM, Shah B, Borre ED, Raitz G, Goode A, Yapa R, Davis JK, Lallinger K, Schmidt R, Kosinski AS, Sanders GD (December 2018). "Interventions for Preventing Thromboembolic Events in Patients With Atrial Fibrillation: A Systematic Review". Annals of Internal Medicine. 169 (11): 774–787. doi:10.7326/M18-1523. PMC 6825839 . PMID 30383133.
- ^ "Atrial fibrillation and new oral anticoagulant drugs". U.S. Food and Drug Administration (FDA). 2 December 2015. Diakses tanggal 22 April 2020.
- ^ "Atrial fibrillation, oral anticoagulant drugs, and their reversal agents". U.S. Food and Drug Administration. 2 December 2015. Diakses tanggal 22 April 2020.
- ^ "No change is needed in use of direct oral anticoagulants following EMA-funded study". European Medicines Agency (EMA). 27 March 2020. Diakses tanggal 22 April 2020.
- ^ "Andexxa- andexanet alfa injection, powder, lyophilized, for solution". DailyMed. 8 January 2019. Diakses tanggal 23 December 2019.
- ^ "Andexxa (coagulation factor Xa (recombinant), inactivated-zhzo)". U.S. Food and Drug Administration (FDA). 31 December 2018. Diakses tanggal 22 April 2020.
- ^ Frost C, Wang J, Nepal S, Schuster A, Barrett YC, Mosqueda-Garcia R, Reeves RA, LaCreta F (February 2013). "Apixaban, an oral, direct factor Xa inhibitor: single dose safety, pharmacokinetics, pharmacodynamics and food effect in healthy subjects". British Journal of Clinical Pharmacology. 75 (2): 476–487. doi:10.1111/j.1365-2125.2012.04369.x. PMC 3558798 . PMID 22759198.
- ^ "2019 First Generic Drugs Approvals". U.S. Food and Drug Administration (FDA). 5 August 2020. Diarsipkan dari versi asli tanggal 30 June 2023. Diakses tanggal 30 June 2023.
- ^ "Bristol-Myers Squibb Co. v. Aurobindo Pharma USA Inc." JD Supra. Diakses tanggal 30 November 2021.
- ^ "Bristol Myers, Pfizer fend off a key challenge to their top-selling heart drug". BioPharma Dive. Diakses tanggal 30 November 2021.
- ^ "Federal Circuit Crystallizes BMS' Apixaban District Court Win". The National Law Review. Diakses tanggal 30 November 2021.
- ^ Levy S (1 August 2022). "Apotex offers generic Eliquis in Canada". Drugstore News. Diakses tanggal 2 September 2022.
- ^ "First Generic Alternative to Eliquis Now Available in Canada". Apotex (Siaran pers). 20 July 2022. Diakses tanggal 29 June 2023.
- ^ Kansteiner, Fraiser (29 August 2023). "Drugs from J&J, Merck, Novartis, BMS and more set for first round of Medicare price negotiations: CMS". Diakses tanggal 31 August 2023.
- ^ Lovelace Jr., Berkeley (15 August 2024). "Medicare announces lower prices on 10 common, high-cost drugs". NBC News (dalam bahasa Inggris). Diakses tanggal 21 August 2024.
- ^ "Medicare Drug Price Negotiation Program: Medicare Prices Negotiated for 2026 Compared to List and U.S. Market Prices" (PDF). Office of the Assistant Secretary for Planning and Evaluation, U.S. Department of Health and Human Services. 15 August 2024.