Dinatrium hidrogen fosfat
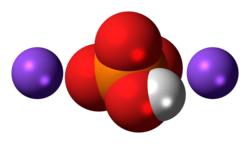
Dinatrium fosfat (DSP), atau dinatrium hidrogen fosfat, atau natrium fosfat dibasa, adalah senyawa anorganik dengan rumus kimia Na
2HPO
4. Senyawa ini merupakan salah satu dari beberapa natrium fosfat. Garam ini dikenal dalam bentuk anhidrat dan juga menghidrasi Na
2HPO
4 · nH
2O, dengan n adalah 2, 7, 8, dan 12. Semuanya berupa bubuk putih yang larut dalam air. Garam anhidrat bersifat higroskopis.[1]

| |
 | |

| |
| Nama | |
|---|---|
Nama lain
| |
| Penanda | |
| |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII |
|
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| Na 2HPO 4 | |
| Massa molar |
|
| Penampilan | Padatan kristal putih |
| Bau | tak berbau |
| Densitas | 1,7 g/cm3 |
| Titik lebur | 250 °C (482 °F; 523 K) Terurai |
| 7,7 g/(100 ml) (20 °C) 11,8 g/(100 ml) (25 °C, heptahidrat) | |
| Kelarutan | Tidak larut dalam etanol |
| log P | −5,8 |
| Keasaman (pKa) | 12,35 |
| −56,6·10−6 cm3/mol | |
| Indeks bias (nD) | 1,35644 — 1,35717 pada suhu 20°C |
| Bahaya | |
| Bahaya utama | Pengiritasi |
| Lembar data keselamatan | ICSC 1129 |
| Titik nyala | Tidak mudah terbakar |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
17000 mg/kg (pada tikus, secara oral) |
| Senyawa terkait | |
Anion lain
|
natrium fosfit |
Kation lainnya
|
Dikalium fosfat Diamonium fosfat |
Senyawa terkait
|
Mononatrium fosfat Trinatrium fosfat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
pH larutan air dinatrium hidrogen fosfat berada di antara 8,0 dan 11,0, yang berarti bersifat agak basa:
HPO2−
4 + H
2O ⇌ H
2PO−
4 + OH−
Produksi dan reaksi
suntingSenyawa ini dapat dihasilkan dengan menetralkan asam fosfat dengan natrium hidroksida:
H
3PO
4 + 2 NaOH → Na
2HPO
4 + 2 H
2O
Secara industri, senyawa ini dibuat dalam proses dua langkah dengan mengolah dikalsium fosfat dengan natrium bisulfat, yang menghasilkan endapan kalsium sulfat:[2]
CaHPO
4 + NaHSO
4 → NaH
2PO
4 + CaSO
4
Pada langkah kedua, larutan mononatrium fosfat yang dihasilkan dinetralkan sebagian:
NaH
2PO
4 + NaOH → Na
2HPO
4 + H
2O
Kegunaan
suntingZat ini digunakan bersama dengan trinatrium fosfat dalam makanan dan pengolahan pelunakan air. Dalam makanan, zat ini digunakan untuk mengatur pH. Keberadaannya mencegah koagulasi dalam pembuatan susu kental manis. Demikian pula, zat ini digunakan sebagai aditif anti-penggumpalan dalam produk bubuk.[3] Zat ini digunakan dalam makanan penutup dan puding, misalnya Cream of Wheat untuk mempercepat waktu memasak, dan puding instan Jell-O untuk mengentalkan. Dalam pengolahan air, zat ini menghambat pembentukan kerak kalsium.[butuh rujukan] Zat ini juga ditemukan dalam beberapa deterjen dan bahan pembersih.[2]
Pencahar
suntingNatrium fosfat monobasa dan dibasa digunakan sebagai pencahar garam untuk mengobati sembelit atau untuk membersihkan usus sebelum kolonoskopi.[4]
Referensi
sunting- ^ "Physical data (pdf)" (PDF). Diarsipkan dari versi asli (PDF) tanggal 2011-07-17. Diakses tanggal 2007-03-06.
- ^ a b Klaus Schrödter, Gerhard Bettermann, Thomas Staffel, Friedrich Wahl, Thomas Klein, Thomas Hofmann "Phosphoric Acid and Phosphates" in Ullmann’s Encyclopedia of Industrial Chemistry 2008, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a19_465.pub3
- ^ "MSDS". Diarsipkan dari versi asli tanggal 2017-10-28. Diakses tanggal 2011-09-26.
- ^ "Sodium Phosphate, Dibasic, Sodium Phosphate, Monobasic Oral solution". Krames Patient Education. Diarsipkan dari versi asli tanggal 2013-01-28. Diakses tanggal 2009-10-29.
Pranala luar
sunting- Media tentang Disodium phosphate di Wikimedia Commons solubility in Prophylaxis alcohol