Tetrametoksimetana
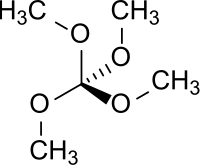
Tetrametoksimetana adalah sebuah senyawa kimia yang secara formal dibentuk melalui metilasi lengkap asam ortokarbonat hipotetis C(OH)4 (asam ortokarboksilat melanggar aturan Erlenmeyer dan tidak stabil dalam keadaan bebas).
| |
| Nama | |
|---|---|
| Nama IUPAC (preferensi)
Tetrametoksimetana | |
| Nama lain
Tetrametil ortokarbonat
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
| Nomor UN | 3272 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C5H12O4 | |
| Massa molar | 136,15 g·mol−1 |
| Penampilan | Cairan nirwarna[1] |
| Densitas | 1,023 g/cm3 (25 °C) |
| Titik lebur | −5,5 °C[1] |
| Titik didih | 114 °C[1] |
| Bahaya | |
| Piktogram GHS |  
|
| Keterangan bahaya GHS | {{{value}}} |
| H225, H315, H319, H335 | |
| P210, P261, P305+351+338 | |
| Senyawa terkait | |
Kation lainnya
|
Tetrametoksisilana |
Senyawa terkait
|
Tetraetoksimetana |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Pembuatan
suntingRute sintetik yang jelas dari tetraklorometana tidak menghasilkan produk yang diinginkan.[2] Oleh karena itu, pembuatan tetrametoksimetana pertama didasarkan pada kloropikrin:[1]
Karena sifat kloropikrin yang tidak mengenakkan, turunan metana reaktif tetrasubstitusi lainnya diselidiki sebagai bahan awal untuk tetrametoksimetana. Misalnya, triklorometanasulfenil klorida (juga digunakan sebagai senjata kimia dan mudah diperoleh dari karbon bisulfida dan klorin):[3][4]
Sintesis yang tidak terlalu bermasalah didasarkan pada trikloroasetonitril,[5][6] dengan hasil yang dapat dicapai sekitar 70%:
Metode pembuatan lebih lanjut telah dijelaskan dalam literatur berikut.[7]
Sifat
suntingTetrametoksimetana adalah cairan jernih, berbau aromatik, dengan viskositas rendah yang stabil terhadap pembentukan peroksida.[8]
Kegunaan
suntingSelain digunakan sebagai pelarut, tetrametoksimetana digunakan sebagai bahan bakar dalam sel bahan bakar polimer,[9] sebagai zat alkilasi pada suhu tinggi (180–200 °C),[10] sebagai reagen transesterifikasi (tetapi menunjukkan reaktivitas yang lebih rendah dibandingkan trimetoksimetana[2]), dan sebagai reagen untuk sintesis 2-aminobenzoksazola, yang digunakan sebagai blok penyusun molekuler dalam bahan aktif farmasi yang digunakan dalam neuroleptik, obat penenang, antimuntah, pelemas otot, fungisida, dan lain-lain.[11]
Tergantung pada substituennya, reaksi satu pot berlangsung dengan hasil yang "sederhana hingga sangat baik".
Referensi
sunting- ^ a b c d H. v. Hartel, Über Existenz und Darstellung des Orthokohlensäure-tetramethylesters, Ber.dtsch.chem.Ges., 60(8), 1841 (1927), DOI:10.1002/cber.19270600821.
- ^ a b R. H. De Wolfe, Carboxylic ortho acid derivatives: preparation and synthetic applications, Organic Chemistry, Vol. 14, Academic Press, Inc. New York – London, 1970, ISBN 978-0-12-214550-6.
- ^ H. Tieckelmann, H. W. Post, The preparation of methyl, ethyl, propyl, and butyl orthocarbonates, J. Org. Chem., 13 (2), 265-267 (1948), DOI:10.1021/jo01160a014.
- ^ US-Patent US 4,059,656, Processes for neutralizing 2,3-dibromopropanol phosphoric acid esters contained in tris(2,3-dibromo-1-propyl) phosphate, Erfinder: M. Demarcq, Anmelder: Produits Chimiques Ugine Kuhlmann, erteilt am 22. November 1974.
- ^ US-Patent US 3,876,708, Orthocarbonic acid esters, Erfinder: R. Speh, W. Kantlehner, Anmelder: Akzo B.V., erteilt am 8. April 1975.
- ^ US-Patent US 6,825,385 B2, Process for the preparation of orthocarbonates, Erfinder: G. Fries, J. Kirchhoff, Anmelder: Degussa AG, erteilt am 30. November 2004.
- ^ W. Kantlehner et al., Die präparative Chemie der O- und N-funktionellen Orthokohlensäure-Derivate, Synthesis; 1977(2): 73-90, DOI:10.1055/s-1977-24283.
- ^ K. R. Kopecky; J. Molina (1987). "Bis(dimethoxymethyl) peroxide and bis(1,1-dimethoxyethyl) peroxide". Canadian Journal of Chemistry. 65 (10): 2350. doi:10.1139/v87-392.
- ^ US-Patent US 6,864,001, Tetramethyl orthocarbonate fuel cells and systems and methods related thereto, Erfinder: J. Zhang, K. Colbow, Anmelder: Ballard Power Systems Inc., erteilt am 8. März 2005.
- ^ M. Selva et al., Esters and Orthoesters as Alkylating Agents at High Temperature. Applications to Continuous-flow Processes, J. Chem. Soc., Perkin Trans. 2, 519 (1992), DOI:10.1039/P29920000519.
- ^ C. L. Cioffi et al., Synthesis of 2-Aminobenzoxazoles Using Tetramethyl Orthocarbonate or 1,1-Dichloro-diphenoxymethane, J. Org. Chem., 75 (2), 7942-7945 (2010), DOI:10.1021/jo1017052.