Asam lipoat
Artikel ini membutuhkan rujukan tambahan agar kualitasnya dapat dipastikan. |
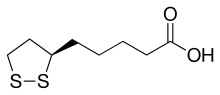
Asam lipoat (bahasa Inggris: Lipoic acid, α-lipoic acid, Alpha Lipoic Acid, thioctic acid, 6,8-dithio-octanoic acid, 1,2-dithiolane-3-pentanoic acid, ALA, LA) adalah senyawa organosulfur yang merupakan turunan dari asam oktanoat dan sisteina yang disekresi oleh hati.[1] Senyawa LA pertama kali ditemukan pada tahun 1950 dari organ hati hewan sapi. Awalnya, oleh karena peran LA pada proses biokimiawi, LA digolongkan menjadi salah satu vitamin di dalam jajaran vitamin B kompleks, tetapi kini tidak lagi demikian.
| |
| |
| Nama | |
|---|---|
| Nama IUPAC
(R)-5-(1,2-dithiolan-3-yl)pentanoic acid
| |
| Nama lain
α-lipoic acid (alpha lipoic acid), thioctic acid, 6,8-dithiooctanoic acid
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
| KEGG | |
| MeSH | Lipoic+acid |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C8H14O2S2 | |
| Massa molar | 206.33 g/mol |
| Penampilan | yellow needle-like crystals |
| soluble in ethanol, sodium salt is soluble in water | |
| Senyawa terkait | |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Asupan nutrisi
Kadar plasma LA endogenus dilaporkan sekitar 1–25 ng/mL, dan DHLA sekitar 33–145 ng/mL. Pada umumnya hati mampu memproduksi cukup LA untuk memenuhi kebutuhan akan senyawa kofaktor enzim dehidrogenase glutarat-alfa dan dehidrogenase piruvat[2] yang berada di dalam mitokondria, namun biosintesis LA lambat laun menurun sejalan dengan usia dan pada penderita beberapa penyakit seperti diabetes, nefropati diabetik dan neuropati diabetik.
Pada penyakit metabolik gabungan malonik dan metilmalonik aciduria (CMAMMA) akibat defisiensi ACSF3, sintesis asam lemak mitokondria (mtFASII), yang merupakan reaksi prekursor biosintesis asam lipoat, terganggu.[3][4] Hasilnya adalah berkurangnya tingkat lipoylasi enzim mitokondria yang penting seperti kompleks piruvat dehidrogenase (PDC) dan kompleks α-ketoglutarat dehidrogenase (α-KGDH).[4] Suplementasi dengan asam lipoat tidak mengembalikan fungsi mitokondria.[5][4]
Oleh sebab itu LA juga merupakan antioksidan yang banyak dikonsumsi, dan segera terkonversi oleh NAD+ atau NADP menjadi bentuk senyawa reduksi yang disebut asam dihidrolipoat (DHLA). Kedua status redoks senyawa LA dan DHLA merupakan antioksidan, hal ini berbeda dengan sifat senyawa lain seperti glutathion yang berfungsi sebagai antioksidan hanya pada status reduksi saja.
LA memiliki 2 isomer yaitu R-enantiomer dan S-enantiomer. R-LA (bahasa Inggris: [(R)-5-(1,2-dithiolan-3-yl)pentanoic acid) dapat ditemukan pada banyak makanan yang mengandung sejenis protein yang disebut lisina. Ikatan kovalen yang dibentuk antara kedua senyawa tersebut menghasilkan senyawa yang disebut lipolisina, yang banyak ditemukan pada bahan nabati seperti horenso, brokoli, tomat, garden peas, brussel sprouts, rice bran, dan khamir;[6] dan bahan hewani seperti jantung, hati dan ginjal.
Aspek manfaat
LA meningkatkan regulasi atas gula darah dan polineuropati yang terkait dengan diabetes mellitus, selain itu, juga, dengan efektif menghilangkan pengaruh keracunan akibat logam berat. LA yang terikat dengan lisina berfungsi sebagai kofaktor bagi enzim kompleks dehidrogenase di dalam mitokondria.
Sebagai antioksidan, LA secara langsung menekan radikal bebas dan dengan kapasitas untuk membungkus senyawa logam, LA secara langsung menekan produksi ROS. Interaksi antara LA dengan antioksidan lain akan mengembalikan/meningkatkan kadar antioksidan tersebut termasuk glutathion dan vitamin C, E, terutama di dalam sitoplasma sel. Hal ini dimungkinkan oleh salah satu sifat LA sebagai senyawa hidrofilik, hidrofobik dan amfifilik hingga memungkinkan aktivitas di dalam fase aqeous intraselular, fase lipid membran plasma, serum dan lipoprotein, dibandingkan dengan vitamin C yang bersifat hidrofilik dan vitamin E yang bersifat hidrofobik.
Diabetes mellitus
Diabetes mellitus sangat terkait dengan stres oksidatif yang terjadi sebagai konsekuensi peningkatan produksi radikal bebas atau penurunan pertahanan antioksidan. Banyak lintasan metabolisme seperti glikasi protein, lintasan poliol, aktivasi protein kinase C dan otooksidasi glukosa yang berdampak pada simtoma hiperglisemia, merupakan akibat dari meningkatnya spesi oksigen reaktif.
Stress oksidatif tidak hanya berkait dengan komplikasi diabetes, tetapi juga berkait dengan resistansi insulin.
Dalam hal ini, LA memiliki potensi untuk mencegah maupun meredakan efek yang ditimbulkan diabetes tipe 1 dan tipe 2. Pada percobaan pada hewan yang menderita diabetes setelah diinduksi oleh cyclophosphamide, pemberian LA secara intraperitoneal dengan dosis 10 mg/kg berat tubuh selama 10 hari, menunjukkan penurunan gejala diabetes yang dimungkinkan oleh penekanan terhadap makrofaga dan pemanfaatan gula darah melalui mekanisme peningkatan translokasi GLUT4 menuju permukaan sel.
Neuropati diabetik
Selama ini, peroksidasi lipid pada membrana saraf dianggap sebagai sebuah mekanisme yang berakibat pada iskemia dan hipoksia dalam sistem saraf. Pada percobaan pada penderita neuropati diabetik dengan asupan LA sebanyak 600 mg/hari diketahui terjadi peningkatan serum seruloplasmin yang disimpulkan sebagai indikasi terbentuknya pertahanan antioksidan, dan penurunan drastis kadar kadar serum lipid peroksida.
Hipertrigliseridemia
Pada percobaan pada tikus yang diinduksi Zucker Diabetic Fatty, asupan R-LA dengan dosis 200 mg/kg/hari selama 5 minggu, menurunkan kadar trigliserida di dalam plasma darah dan hati, dengan penghambatan ekspresi genetik lipogenik hepatik seperti enzim sn-glycerol-3-phosphate acyltransferase-1 (GPAT-1) dan diacylglycerol O-acyltransferase-2 (DGAT-2), sekresi VLDL dan stimulasi daur (bahasa Inggris: clearance) lipoprotein yang kaya akan trigliserida, dan peningkatan glikogen.[7] Hal ini disimpulkan bahwa asupan karbohidrat akan cenderung disimpan sebagai glikogen daripada sebagai substrat lipogenik. Tidak tampak perubahan atau penurunan ekspresi pencerap hepatik peroxisome proliferator activated receptor α yang berperan dalam oksidasi-β asam lemak, menunjukkan bahwa LA memiliki model aktivitas yang berbeda dengan asam fibrat.
Defisiensi endotelium
Disfungsi jaringan endotelium yang disebabkan oleh defisiensi sel endotelial yang membentuknya, disebabkan oleh berbagai faktor risiko kardiovaskular melalui mekanisme yang demikian kompleks yang berujung pada inisiasi dan perkembangan aterosklerosis.[8] Terapi jangka pendek dengan LA, seperti dikutip oleh British Journal of Pharmacology, dapat memperbaiki fungsi endotelial pada cincin aortik seekor tikus. Lebih lanjut disebutkan bahwa penurunan reaksi fosforilasi pada sintase NO dan Akt yang biasa terjadi pada usia lanjut, dapat pula ditingkatkan dengan suplementasi LA yang menginduksi penurunan aktivitas fosfatase PPA-2.
Aktivitas sfingomielinase juga diredam oleh LA, yang pada akhirnya, setidaknya akan meningkatkan kadar glutathion di dalam sel endotelial.
Kontraindikasi
Hingga saat ini belum ditemukan efek samping konsumsi LA dosis rendah, misalnya 5 mg/hari. Kendati demikian, dosis yang lebih tinggi dapat menyebabkan nausea, stomach upset, lelah, dan insomnia, rasa sakit pada abdomen, mual, diare, reaksi anafilaktik seperti laryngospasm, alergi kulit. Malodorous urine dilaporkan pada konsumen dengan dosis 1200 mg/hari, tetapi dosis 600 mg/hari merupakan dosis yang dianjurkan pada penderita diabetes dengan pengamatan kadar gula yang ketat meskipun belum terdapat laporan bahwa LA menginduksi simtoma hipoglisemia, namun kemungkinan tersebut bisa terjadi.
Lihat pula
Rujukan
- ^ (Inggris) "Alpha-lipoic acid supplementation and diabetes". Laboratory of Atherosclerosis and Metabolic Research, Department of Pathology and Laboratory Medicine, UC Davis Medical Center; Uma Singh dan Ishwarlal Jialal. Diakses tanggal 2011-05-16.
- ^ (Inggris) "Lipoic acid effects on established atherosclerosis". Davis Heart Lung Research Institute, bDivision of Environmental Health Sciences, Colleges of Medicine and Public Health, the Ohio State University; Zhekang Ying, Nisharahmed Kherada, Britten Farrar, Thomas Kampfrath, Yiucho Chung, Orlando Simonetti, Jeffrey Deiuliis, Rajagopal Desikan, Bobby Khan, Frederick Villamena, Qinghua Sun, Sampath Parthasarathy, dan Sanjay Rajagopalan. Diakses tanggal 2011-07-14.
- ^ Levtova, Alina; Waters, Paula J.; Buhas, Daniela; Lévesque, Sébastien; Auray‐Blais, Christiane; Clarke, Joe T.R.; Laframboise, Rachel; Maranda, Bruno; Mitchell, Grant A. (2019-01). "Combined malonic and methylmalonic aciduria due to ACSF3 mutations: Benign clinical course in an unselected cohort". Journal of Inherited Metabolic Disease (dalam bahasa Inggris). 42 (1): 107–116. doi:10.1002/jimd.12032. ISSN 0141-8955.
- ^ a b c Wehbe, Zeinab; Behringer, Sidney; Alatibi, Khaled; Watkins, David; Rosenblatt, David; Spiekerkoetter, Ute; Tucci, Sara (2019-11). "The emerging role of the mitochondrial fatty-acid synthase (mtFASII) in the regulation of energy metabolism". Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids (dalam bahasa Inggris). 1864 (11): 1629–1643. doi:10.1016/j.bbalip.2019.07.012.
- ^ Hiltunen, J. Kalervo; Autio, Kaija J.; Schonauer, Melissa S.; Kursu, V.A. Samuli; Dieckmann, Carol L.; Kastaniotis, Alexander J. (2010-06). "Mitochondrial fatty acid synthesis and respiration". Biochimica et Biophysica Acta (BBA) - Bioenergetics (dalam bahasa Inggris). 1797 (6-7): 1195–1202. doi:10.1016/j.bbabio.2010.03.006.
- ^ (Inggris) "Lipoic Acid Synthesis and Attachment in Yeast Mitochondria". Molecular and Cellular Biology, University of Arizona, Department of Biochemistry and Biocenter Oulu, University of Oulu; Melissa S. Schonauer, Alexander J. Kastaniotis, V. A. Samuli Kursu, J. Kalervo Hiltunen, dan Carol L. Dieckmann. Diakses tanggal 2011-05-17.
Through analysis of the role of these genes in protein lipoylation, we conclude that only one pathway for de novo synthesis and attachment of lipoic acid exists in yeast.
- ^ (Inggris) "Lipoic acid improves hypertriglyceridemia by stimulating triacylglycerol clearance and downregulating liver triacylglycerol secretion". Linus Pauling Institute, Oregon State University, Department of Biochemistry and Biophysics, Oregon State University; Judy A. Butler, Tory M. Hagen, dan Régis Moreau. Diakses tanggal 2011-05-17.
- ^ (Inggris) "Lipoic acid supplementation and endothelial function". Department of Medicine, Montreal Heart Institute, University of Montreal; J-C Tardif1 dan E Rhéaume. Diakses tanggal 2011-05-17.