Karbidopa
Karbidopa adalah obat yang diberikan kepada penderita penyakit Parkinson untuk menghambat metabolisme perifer levodopa. Khasiat ini penting karena memungkinkan sebagian besar levodopa yang diberikan untuk melewati sawar darah otak untuk memberikan efek pada sistem saraf pusat, alih-alih dimetabolisme secara perifer menjadi zat yang tidak dapat melewati sawar tersebut.

| |
|---|---|
| |
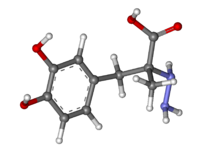
| Nama sistematis (IUPAC) | |
| (2S)-3-(3,4-dihidroksifenil)-2-hidrazino-2-asam metilpropanoat | |
| Data klinis | |
| Nama dagang | Lodosyn |
| AHFS/Drugs.com | monograph |
| Data lisensi | EMA:pranala, US FDA:link |
| Kat. kehamilan | ? |
| Status hukum | POM (UK) ℞-only (US) |
| Data farmakokinetik | |
| Ikatan protein | 76% |
| Metabolisme | 7 metabolit diketahui, tidak dimetabolisme secara ekstensif |
| Waktu paruh | 2 jam |
| Pengenal | |
| Nomor CAS | 28860-95-9 |
| Kode ATC | ? |
| PubChem | CID 34359 |
| Ligan IUPHAR | 5159 |
| DrugBank | DB00190 |
| ChemSpider | 31640 |
| UNII | KR87B45RGH |
| KEGG | D00558 |
| ChEBI | CHEBI:39585 |
| ChEMBL | CHEMBL1201236 |
| Data kimia | |
| Rumus | C10H14N2O4 |
| SMILES | eMolecules & PubChem |
| |
| Data fisik | |
| Titik lebur | 203–205 °C (397–401 °F) |
Farmakologi
Karbidopa menghambat dekarboksilase L-asam amino aromatik (DOPA dekarboksilase atau DDC),[1] enzim yang penting dalam biosintesis serotonin dari L-triptofan dan dalam biosintesis dopamin (DA) dari L-DOPA. DDC ada di luar (pinggiran tubuh) dan di dalam batas sawar darah otak.
Karbidopa antara lain digunakan dalam pengobatan penyakit Parkinson (PD), suatu kondisi yang ditandai dengan kematian neuron dopaminergik di substansia nigra. Peningkatan ketersediaan dopamin dapat meningkatkan efektivitas neuron yang tersisa dan meringankan gejala untuk sementara waktu. Tujuan farmakologisnya adalah untuk memasukkan prekursor dopamin eksogen yang dikenal sebagai levodopa/L-DOPA ke dalam otak pasien PD yang kekurangan dopamin. Levodopa/L-DOPA dapat melewati sawar darah otak, tetapi dopamin tidak. Penggunaan karbidopa tampaknya berlawanan dengan intuisi pada penyakit Parkinson (PD) karena mencegah konversi DDC dari levodopa/L-DOPA menjadi dopamin. Namun, jika diberikan secara eksogen, levadopa/L-DOPA dimetabolisme secara perifer menjadi metabolit aktifnya dopamin sebelum mencapai sawar darah otak. Oleh karena itu, otak PD, yang kekurangan dopamin, tidak akan menerima banyak prekursor bakal obat levodopa/L-DOPA karena kerusakan DDC perifer. Namun, karbidopa dapat menurunkan konversi DDC perifer dari levodopa/L-DOPA sebelum melewati sawar darah otak. Karbidopa bertindak sebagai penghambat DDC perifer, karena karbidopa sendiri tidak dapat melewati sawar darah otak. Dengan kata lain, karbidopa tidak memiliki efek pada konversi DDC otak dari levodopa/L-DOPA menjadi dopamin. Pada akhirnya, proporsi yang lebih besar dari levodopa/L-DOPA yang diberikan secara eksogen mencapai otak. Secara komersial, kombinasi karbidopa/levodopa tersedia dalam pengobatan defisiensi dopamin sentral.
Bersama karbidopa, penghambat DDC lainnya adalah benserazid (Ro-4-4602), difluorometildopa, dan α-metildopa.
Sintesis
Sintesis diawali dengan reaksi Strecker yang dimodifikasi menggunakan hidrazina dan kalium sianida pada arilaseton (1) untuk menghasilkan 2. Zat ini kemudian dihidrolisis dengan HCl dingin untuk menghasilkan karboksamida 3. Hidrolisis yang lebih kuat dengan 48% HBr memecah ikatan amida dan gugus aril eter untuk menghasilkan karbidopa (4).
Referensi
- ^ Gilbert JA, Frederick LM, Ames MM (November 2000). "The aromatic-L-amino acid decarboxylase inhibitor carbidopa is selectively cytotoxic to human pulmonary carcinoid and small cell lung carcinoma cells". Clinical Cancer Research. 6 (11): 4365–4372. PMID 11106255.
- ^ Sletzinger M, Chemerda JM, Bollinger FW (March 1963). "Potent Decarboxylase Inhibitors. Analogs of Methyldopa". Journal of Medicinal Chemistry. 6 (2): 101–103. doi:10.1021/jm00338a003. PMID 14188777.
- ^ Karady S, Ly MG, Pines SH, Sletzinger M (1971). "Synthesis of D- and L-α-(3,4-dihydroxybenzyl)-α-hydrazinopropionic acid via resolution". The Journal of Organic Chemistry. 36 (14): 1946–1948. doi:10.1021/jo00813a023.
- ^ Karady S, Ly MG, Pines SH, Sletzinger M (1971). "Synthesis of L-α-(3,4-dihydroxybenzyl)-α-hydrazinopropionic acid from optically active precursors by N-homologization". The Journal of Organic Chemistry. 36 (14): 1949–1951. doi:10.1021/jo00813a024.
- ^ GB 940596, Chemerda JM, Sletzinger M, Bollinger FW, "α-hydrazino acids", diterbitkan tanggal 1963-10-30, diberikan kepada Merck & Co. Inc.
- ^ DE 2062285, Karady S, Pines SH, Ly MG, Sletzinger M, Allegretti JE, Wildman Jr AS, "L-α-Hydrazino-β-phenylpropionsäure-Verbindungen enthaltendes Arzneimittel [L-alpha-hydrazino-beta-phenylpropionic acid compounds, decarboxylase inhibitors]", diterbitkan tanggal 1971-07-01, diberikan kepada Merck & Co. Inc.
- ^ DE 2062332, Karady S, Pines SH, Ly MG, Sletzinger M, Allegretti JE, Wildman Jr AS, "L-α-Hydrazino-β-phenylpropionsäure-Verbindungen und Verfahren zu deren Herstellung[L-alpha-hydrazino-beta-phenylpropionic acid compounds and processes for their preparation]", diterbitkan tanggal 1971-07-15, diberikan kepada Merck & Co. Inc.