Enzim
Enzim adalah biomolekul berupa protein yang berfungsi sebagai katalis (senyawa yang mempercepat proses reaksi tanpa habis bereaksi) dalam suatu reaksi kimia organik.[1][2] Molekul awal yang disebut substrat akan dipercepat perubahannya menjadi molekul lain yang disebut produk. Semua proses biologis sel memerlukan enzim agar dapat berlangsung dengan cukup cepat dalam suatu arah lintasan metabolisme.

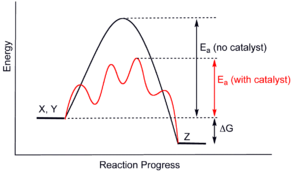
Enzim bekerja dengan cara bereaksi dengan molekul substrat untuk menghasilkan senyawa intermediat melalui suatu reaksi kimia organik yang membutuhkan energi aktivasi lebih rendah, sehingga percepatan reaksi kimia terjadi karena reaksi kimia dengan energi aktivasi lebih tinggi membutuhkan waktu lebih lama. Sebagai contoh:
- X + C → XC (1)
- Y + XC → XYC (2)
- XYC → CZ (3)
- CZ → C + Z (4)
Meskipun senyawa katalis dapat berubah pada reaksi awal, pada reaksi akhir molekul katalis akan kembali ke bentuk semula.
Sebagian besar enzim bekerja secara khas, yang artinya setiap jenis enzim hanya dapat bekerja pada satu macam senyawa atau reaksi kimia. Hal ini disebabkan perbedaan struktur kimia tiap enzim yang bersifat tetap. Sebagai contoh, enzim α-amilase hanya dapat digunakan pada proses perombakan pati menjadi glukosa.
Kerja enzim dipengaruhi oleh beberapa faktor, terutama adalah substrat, suhu, keasaman, kofaktor dan inhibitor. Tiap enzim memerlukan suhu dan pH (tingkat keasaman) optimum yang berbeda-beda karena enzim adalah protein, yang dapat mengalami perubahan bentuk jika suhu dan keasaman berubah. Di luar suhu atau pH yang sesuai, enzim tidak dapat bekerja secara optimal atau strukturnya akan mengalami kerusakan. Hal ini akan menyebabkan enzim kehilangan fungsinya sama sekali. Kerja enzim juga dipengaruhi oleh molekul lain. Inhibitor adalah molekul yang menurunkan aktivitas enzim, sedangkan aktivator adalah yang meningkatkan aktivitas enzim. Banyak obat dan racun adalah inihibitor enzim.
Etimologi dan Sejarah
Hal-ihwal yang berkaitan dengan enzim dipelajari dalam enzimologi. Dalam dunia pendidikan tinggi, enzimologi tidak dipelajari tersendiri sebagai satu jurusan tersendiri tetapi sejumlah program studi memberikan mata kuliah ini. Enzimologi terutama dipelajari dalam kedokteran, ilmu pangan, teknologi pengolahan pangan, dan cabang-cabang ilmu pertanian.
Pada akhir tahun 1700-an dan awal tahun 1800-an, pencernaan daging oleh sekresi lambung[3] dan konversi pati menjadi gula oleh ekstrak tumbuhan dan ludah telah diketahui. Namun, mekanisme bagaimana hal ini terjadi belum diidentifikasi.[4]
Pengetahuan tentang enzim telah dirintis oleh Berzelius pada tahun 1837. Ia mengusulkan nama "katalis" untuk zat-zat yang dapat mempercepat reaksi tetapi zat itu sendiri tidak ikut bereaksi. Namun, proses kimia yang terjadi dengan pertolongan enzim telah dikenal sejak zaman dahulu misalnya pembuatan anggur dengan cara fermentasi atau peragian, dan pembuatan asam cuka. Lois Pasteur salah seorang yang banyak bekerja dalam fermentasi ini dan ketika mengkaji fermentasi gula menjadi alkohol oleh ragi, Louis Pasteur menyimpulkan bahwa fermentasi ini dikatalisasi oleh gaya dorong vital yang terdapat dalam sel ragi, disebut sebagai "ferment", dan diperkirakan hanya berfungsi dalam tubuh organisme hidup. Ia menulis bahwa "fermentasi alkoholik adalah peristiwa yang berhubungan dengan kehidupan dan organisasi sel ragi, dan bukannya kematian ataupun putrefaksi sel tersebut."[5]
Pada tahun 1878, ahli fisiologi Jerman Wilhelm Kühne (1837–1900) pertama kali menggunakan istilah "enzyme", yang berasal dari bahasa Yunani ενζυμον yang berarti "dalam bahan pengembang" (ragi), untuk menjelaskan proses ini. Kata "enzyme" kemudian digunakan untuk merujuk pada zat mati seperti pepsin, dan kata ferment digunakan untuk merujuk pada aktivitas kimiawi yang dihasilkan oleh organisme hidup.
Pada tahun 1897, Eduard Buchner memulai kajiannya mengenai kemampuan ekstrak ragi untuk memfermentasi gula walaupun ia tidak terdapat pada sel ragi yang hidup. Pada sederet eksperimen di Universitas Berlin, ia menemukan bahwa gula difermentasi bahkan apabila sel ragi tidak terdapat pada campuran.[6] Ia menamai enzim yang memfermentasi sukrosa sebagai "zymase" (zimase).[7] Pada tahun 1907, ia menerima penghargaan Nobel dalam bidang kimia "atas riset biokimia dan penemuan fermentasi tanpa sel yang dilakukannya". Mengikuti praktik Buchner, enzim biasanya dinamai sesuai dengan reaksi yang dikatalisasi oleh enzim tersebut. Umumnya, untuk mendapatkan nama sebuah enzim, akhiran -ase ditambahkan pada nama substrat enzim tersebut (contohnya: laktase, merupakan enzim yang mengurai laktosa) ataupun pada jenis reaksi yang dikatalisasi (contoh: DNA polimerase yang menghasilkan polimer DNA).
Penemuan bahwa enzim dapat bekerja di luar sel hidup mendorong penelitian pada sifat-sifat biokimia enzim tersebut. Banyak peneliti awal menemukan bahwa aktivitas enzim diasosiasikan dengan protein, tetapi beberapa ilmuwan seperti Richard Willstätter berargumen bahwa proten hanyalah bertindak sebagai pembawa enzim dan protein sendiri tidak dapat melakukan katalisis. Namun, pada tahun 1926, James B. Sumner berhasil mengkristalisasi enzim urease dan menunjukkan bahwa ia merupakan protein murni. Kesimpulannya adalah bahwa protein murni dapat berupa enzim dan hal ini secara tuntas dibuktikan oleh Northrop dan Stanley yang meneliti enzim pencernaan pepsin (1930), tripsin, dan kimotripsin. Ketiga ilmuwan ini meraih penghargaan Nobel tahun 1946 pada bidang kimia.[8]
Penemuan bahwa enzim dapat dikristalisasi pada akhirnya mengizinkan struktur enzim ditentukan melalui kristalografi sinar-X. Metode ini pertama kali diterapkan pada lisozim, enzim yang ditemukan pada air mata, air ludah, dan telur putih, yang mencerna lapisan pelindung beberapa bakteri. Struktur enzim ini dipecahkan oleh sekelompok ilmuwan yang diketuai oleh David Chilton Phillips dan dipublikasikan pada tahun 1965.[9] Struktur lisozim dalam resolusi tinggi ini menandai dimulainya bidang biologi struktural dan usaha untuk memahami bagaimana enzim bekerja pada tingkat atom.
Konvensi penamaan
Nama enzim sering kali diturunkan dari nama substrat ataupun reaksi kimia yang ia kataliskan dengan akhiran -ase. Contohnya adalah laktase, alkohol dehidrogenase (mengatalisis penghilangan hidrogen dari alkohol), dan DNA polimerase.
International Union of Biochemistry and Molecular Biology telah mengembangkan suatu tatanama untuk enzim, yang disebut sebagai nomor EC; tiap-tiap enzim memiliki empat digit nomor urut sesuai dengan ketentuan klasifikasi yang berlaku. Nomor pertama untuk klasifikasi teratas enzim didasarkan pada ketentuan berikut:
- EC 1 Oksidoreduktase: mengatalisis reaksi oksidasi/reduksi.
- EC 2 Transferase: mentransfer gugus fungsi
- EC 3 Hidrolase: mengatalisis hidrolisis berbagai ikatan
- EC 4 Liase: memutuskan berbagai ikatan kimia selain melalui hidrolisis dan oksidasi
- EC 5 Isomerase: mengatalisis isomerisasi sebuah molekul tunggal
- EC 6 Ligase: menggabungkan dua molekul dengan ikatan kovalen
Tata nama secara lengkap dapat dilihat di http://www.chem.qmul.ac.uk/iubmb/enzyme/ (Bahasa Inggris).
Struktur dan mekanisme
Enzim umumnya merupakan protein globular dan ukurannya berkisar dari hanya 62 asam amino pada monomer 4-oksalokrotonat tautomerase[10], sampai dengan lebih dari 2.500 residu pada asam lemak sintase.[11] Terdapat pula sejumlah kecil katalis RNA, dengan yang paling umum merupakan ribosom; Jenis enzim ini dirujuk sebagai RNA-enzim ataupun ribozim. Aktivitas enzim ditentukan oleh struktur tiga dimensinya (struktur kuaterner).[12] Walaupun struktur enzim menentukan fungsinya, prediksi aktivitas enzim baru yang hanya dilihat dari strukturnya adalah hal yang sangat sulit.[13]
Kebanyakan enzim berukuran lebih besar daripada substratnya, tetapi hanya sebagian kecil asam amino enzim (sekitar 3–4 asam amino) yang secara langsung terlibat dalam katalisis.[14] Daerah yang mengandung residu katalitik yang akan mengikat substrat dan kemudian menjalani reaksi ini dikenal sebagai sisi aktif. Enzim juga dapat mengandung sisi yang mengikat kofaktor yang diperlukan untuk katalisis. Beberapa enzim juga memiliki sisi untuk mengikat molekul kecil, yang sering kali merupakan produk langsung ataupun tak langsung dari reaksi yang dikatalisasi. Pengikatan ini dapat meningkatkan ataupun menurunkan aktivitas enzim. Dengan demikian ia berfungsi sebagai regulasi umpan balik.
Sama seperti protein-protein lainnya, enzim merupakan rantai asam amino yang melipat. Tiap-tiap urutan asam amino menghasilkan struktur pelipatan dan sifat-sifat kimiawi yang khas. Rantai protein tunggal kadang-kadang dapat berkumpul bersama dan membentuk kompleks protein. Kebanyakan enzim dapat mengalami denaturasi (yakni terbuka dari lipatannya dan menjadi tidak aktif) oleh pemanasan ataupun denaturan kimiawi. Tergantung pada jenis-jenis enzim, denaturasi dapat bersifat reversibel maupun ireversibel.
Kespesifikan
Enzim biasanya sangat spesifik terhadap reaksi yang ia kataliskan maupun terhadap substrat yang terlibat dalam reaksi. Bentuk, muatan dan katakteristik hidrofilik/hidrofobik enzim dan substrat bertanggung jawab terhadap kespesifikan ini. Enzim juga dapat menunjukkan tingkat stereospesifisitas, regioselektivitas, dan kemoselektivitas yang sangat tinggi.[15]
Beberapa enzim yang menunjukkan akurasi dan kespesifikan tertinggi terlibat dalam pengkopian dan pengekspresian genom. Enzim-enzim ini memiliki mekanisme "sistem pengecekan ulang". Enzim seperti DNA polimerase mengatalisasi reaksi pada langkah pertama dan mengecek apakah produk reaksinya benar pada langkah kedua.[16] Proses dwi-langkah ini menurunkan laju kesalahan dengan 1 kesalahan untuk setiap 100 juta reaksi pada polimerase mamalia.[17] Mekanisme yang sama juga dapat ditemukan pada RNA polimerase,[18] aminoasil tRNA sintetase[19] dan ribosom.[20]
Beberapa enzim yang menghasilkan metabolit sekunder dikatakan sebagai "tidak pilih-pilih", yakni bahwa ia dapat bekerja pada berbagai jenis substrat yang berbeda-beda. Diajukan bahwa kespesifikan substrat yang sangat luas ini sangat penting terhadap evolusi lintasan biosintetik yang baru.[21]
Model "kunci dan gembok"
Enzim sangatlah spesifik. Pada tahun 1894, Emil Fischer mengajukan bahwa hal ini dikarenakan baik enzim dan substrat memiliki bentuk geometri yang saling memenuhi.[22] Hal ini sering dirujuk sebagai model "Kunci dan Gembok". Manakala model ini menjelaskan kespesifikan enzim, ia gagal dalam menjelaskan stabilisasi keadaan transisi yang dicapai oleh enzim. Model ini telah dibuktikan tidak akurat, dan model ketepatan induksilah yang sekarang paling banyak diterima.
Model ketepatan induksi
Pada tahun 1958, Daniel Koshland mengajukan modifikasi model kunci dan gembok: oleh karena enzim memiliki struktur yang fleksibel, tapak aktif secara terus menerus berubah bentuknya sesuai dengan interaksi antara enzim dan substrat.[23] Akibatnya, substrat tidak berikatan dengan tapak aktif yang kaku. Orientasi rantai samping asam amino berubah sesuai dengan substrat dan mengizinkan enzim untuk menjalankan fungsi katalitiknya. Pada beberapa kasus, misalnya glikosidase, molekul substrat juga berubah sedikit ketika ia memasuki tapak aktif.[24] Tapak aktif akan terus berubah bentuknya sampai substrat terikat secara sepenuhnya, yang mana bentuk akhir dan muatan enzim ditentukan.[25]
Mekanisme
Enzim dapat bekerja dengan beberapa cara, yang kesemuaannya menurunkan ΔG‡:[26]
- Menurunkan energi aktivasi dengan menciptakan suatu lingkungan yang mana keadaan transisi terstabilisasi (contohnya mengubah bentuk substrat menjadi konformasi keadaan transisi ketika ia terikat dengan enzim.)
- Menurunkan energi keadaan transisi tanpa mengubah bentuk substrat dengan menciptakan lingkungan yang memiliki distribusi muatan yang berlawanan dengan keadaan transisi.
- Menyediakan lintasan reaksi alternatif. Contohnya bereaksi dengan substrat sementara waktu untuk membentuk kompleks Enzim-Substrat antara.
- Menurunkan perubahan entropi reaksi dengan menggiring substrat bersama pada orientasi yang tepat untuk bereaksi. Menariknya, efek entropi ini melibatkan destabilisasi keadaan dasar,[27] dan kontribusinya terhadap katalis relatif kecil.[28]
Stabilisasi keadaan transisi
Pemahaman asal usul penurunan ΔG‡ memerlukan pengetahuan bagaimana enzim dapat menghasilkan keadaan transisi reaksi yang lebih stabil dibandingkan dengan stabilitas keadaan transisi reaksi tanpa katalis. Cara yang paling efektif untuk mencapai stabilisasi yang besar adalah menggunakan efek elektrostatik, terutama pada lingkungan yang relatif polar yang diorientasikan ke distribusi muatan keadaan transisi.[29] Lingkungan seperti ini tidak ada dapat ditemukan pada reaksi tanpa katalis di air.
Dinamika dan fungsi
Dinamika internal enzim berhubungan dengan mekanisme katalis enzim tersebut.[30][31][32] Dinamika internal enzim adalah pergerakan bahagian struktur enzim, misalnya residu asam amino tunggal, sekelompok asam amino, ataupun bahwa keseluruhan domain protein. Pergerakan ini terjadi pada skala waktu yang bervariasi, berkisar dari beberapa femtodetik sampai dengan beberapa detik. Jaringan residu protein di seluruh struktur enzim dapat berkontribusi terhadap katalisis melalui gerak dinamik.[33][34][35][36] Gerakan protein sangat vital, tetapi apakah vibrasi yang cepat atau lambat maupun pergerakan konformasi yang besar atau kecil yang lebih penting bergantung pada tipe reaksi yang terlibat. Namun, walaupun gerak ini sangat penting dalam hal pengikatan dan pelepasan substrat dan produk, adalah tidak jelas jika gerak ini membantu mempercepat langkah-langkah reaksi reaksi enzimatik ini.[37] Penyingkapan ini juga memiliki implikasi yang luas dalam pemahaman efek alosterik dan pengembangan obat baru.
Modulasi alosterik
Enzim alosterik mengubah strukturnya sesuai dengan efektornya. Modulasi ini dapat terjadi secara langsung, di mana efektor mengikat tapak ikat enzim secara lngsung, ataupun secara tidak langsung, di mana efektor mengikat protein atau subunit protein lain yang berinteraksi dengan enzim alosterik, sehingga memengaruhi aktivitas katalitiknya.
Kofaktor dan koenzim
Kofaktor
Beberapa enzim tidak memerlukan komponen tambahan untuk mencapai aktivitas penuhnya. Namun beberapa memerlukan pula molekul non-protein yang disebut kofaktor untuk berikatan dengan enzim dan menjadi aktif.[38] Kofaktor dapat berupa zat anorganik (contohnya ion logam) ataupun zat organik (contohnya flavin dan heme). Kofaktor dapat berupa gugus prostetik yang mengikat dengan kuat, ataupun koenzim, yang akan melepaskan diri dari tapak aktif enzim semasa reaksi.
Enzim yang memerlukan kofaktor namun tidak terdapat kofaktor yang terikat dengannya disebut sebagai apoenzim ataupun apoprotein. Apoenzim beserta dengan kofaktornya disebut holoenzim (bentuk aktif). Kebanyakan kofaktor tidak terikat secara kovalen dengan enzim, tetapi terikat dengan kuat. Namun, gugus prostetik organik dapat pula terikat secara kovalen (contohnya tiamina pirofosfat pada enzim piruvat dehidrogenase). Istilah holoenzim juga dapat digunakan untuk merujuk pada enzim yang mengandung subunit protein berganda, seperti DNA polimerase. Pada kasus ini, holoenzim adalah kompleks lengkap yang mengandung seluruh subunit yang diperlukan agar menjadi aktif.
Contoh enzim yang mengandung kofaktor adalah karbonat anhidrase, dengan kofaktor seng terikat sebagai bagian dari tapak aktifnya.[39]
Koenzim
Koenzim adalah kofaktor berupa molekul organik kecil yang mentranspor gugus kimia atau elektron dari satu enzim ke enzim lainnya.[38][40][41] Contoh koenzim mencakup NADH, NADPH dan adenosina trifosfat. Gugus kimiawi yang dibawa mencakup ion hidrida (H–) yang dibawa oleh NAD atau NADP+, gugus asetil yang dibawa oleh koenzim A, formil, metenil, ataupun gugus metil yang dibawa oleh asam folat, dan gugus metil yang dibawa oleh S-adenosilmetionina. Beberapa koenzim seperti riboflavin, tiamina, dan asam folat adalah vitamin.
Oleh karena koenzim secara kimiawi berubah oleh aksi enzim, adalah dapat dikatakan koenzim merupakan substrat yang khusus, ataupun substrat sekunder. Sebagai contoh, sekitar 700 enzim diketahui menggunakan koenzim NADH.[42]
Regenerasi serta pemeliharaan konsentrasi koenzim terjadi dalam sel. Contohnya, NADPH diregenerasi melalui lintasan pentosa fosfat, dan S-adenosilmetionina melalui metionina adenosiltransferase.
Termodinamika
Sebagai katalis, enzim tidak mengubah posisi kesetimbangan reaksi kimia. Biasanya reaksi akan berjalan ke arah yang sama dengan reaksi tanpa katalis. Perbedaannya adalah, reaksi enzimatik berjalan lebih cepat. Namun, tanpa keberadaan enzim, reaksi samping yang memungkinkan dapat terjadi dan menghasilkan produk yang berbeda.
Lebih lanjut, enzim dapat menggabungkan dua atau lebih reaksi, sehingga reaksi yang difavoritkan secara termodinamik dapat digunakan untuk mendorong reaksi yang tidak difavoritkan secara termodinamik. Sebagai contoh, hidrolsis ATP sering kali menggunakan reaksi kimia lainnya untuk mendorong reaksi.
Enzim mengatalisasi reaksi maju dan balik secara seimbang. Enzim tidak mengubah kesetimbangan reaksi itu sendiri, tetapi hanya mempercepat reaksi saja. Sebagai contoh, karbonat anhidrase mengatalisasi reaksinya ke dua arah bergantung pada konsentrasi reaktan.
- (dalam jaringan tubuh; konsentrasi CO2 yang tinggi)
- (pada paru-paru; konsentrasi CO2 yang rendah)
Walaupun demikian, jika kesetimbangan tersebut sangat memfavoritkan satu arah reaksi, yakni reaksi yang sangat eksergonik, reaksi itu akan menjadi ireversible. Pada kondisi demikian, enzim akan hanya mengatalisasi reaksi yang diijinkan secara termodinamik.
Kinetika
Kinetika enzim menginvestigasi bagaimana enzim mengikat substrat dengan mengubahnya menjadi produk. Data laju yang digunakan dalam analisis kinetika didapatkan dari asai enzim.
Pada tahun 1902, Victor Henri[43] mengajukan suatu teori kinetika enzim yang kuantitatif, tetapi data eksperimennya tidak berguna karena perhatian pada konsentrasi ion hidrogen pada saat itu masih belum dititikberatkan. Setelah Peter Lauritz Sørensen menentukan skala pH logaritmik dan memperkenalkan konsep penyanggaan (buffering) pada tahun 1909[44], kimiawan Jerman Leonor Michaelis dan murid bimbingan pascadokotoralnya yang berasal dari Kanada, Maud Leonora Menten, mengulangi eksperimen Henri dan mengkonfirmasi persamaan Henri. Persamaan ini kemudian dikenal dengan nama Kinetika Henri-Michaelis-Menten (kadang-kadang juga hanya disebut kinetika Michaelis-Menten).[45] Hasil kerja mereka kemudian dikembangkan lebih jauh oleh G. E. Briggs dan J. B. S. Haldane. Penurunan persamaan kinetika yang diturunkan mereka masih digunakan secara meluas sampai sekarang .[46]
Salah satu kontribusi utama Henri pada kinetika enzim adalah memandang reaksi enzim sebagai dua tahapan. Pada tahap pertama, subtrat terikat ke enzim secara reversible, membentuk kompleks enzim-substrat. Kompleks ini kadang-kadang disebut sebagai kompleks Michaelis. Enzim kemudian mengatalisasi reaksi kimia dan melepaskan produk.
Enzim dapat mengatalisasi reaksi dengan kelajuan mencapai jutaan reaksi per detik. Sebagai contoh, tanpa keberadaan enzim, reaksi yang dikatalisasi oleh enzim orotidina 5'-fosfat dekarboksilase akan memerlukan waktu 78 juta tahun untuk mengubah 50% substrat menjadi produk. Namun, apabila enzim tersebut ditambahkan, proses ini hanya memerlukan waktu 25 milidetik.[47] Laju reaksi bergantung pada kondisi larutan dan konsentrasi substrat. Kondisi-kondisi yang menyebabkan denaturasi protein seperti temperatur tinggi, konsentrasi garam yang tinggi, dan nilai pH yang terlalu tinggi atau terlalu rendah akan menghilangkan aktivitas enzim. Sedangkan peningkatan konsentrasi substrat cenderung meningkatkan aktivitasnya. Untuk menentukan kelajuan maksimum suatu reaksi enzimatik, konsentrasi substrat ditingkatkan sampai laju pembentukan produk yang terpantau menjadi konstan. Hal ini ditunjukkan oleh kurva kejenuhan di samping. Kejenuhan terjadi karena seiring dengan meningkatnya konsentrasi substrat, semakin banyak enzim bebas yang diubah menjadi kompleks substrate-enzim ES. Pada kelajuan yang maksimum (Vmax), semua tapak aktif enzim akan berikatan dengan substrat, dan jumlah kompleks ES adalah sama dengan jumlah total enzim yang ada. Namun, Vmax hanyalah salah satu konstanta kinetika enzim. Jumlah substrat yang diperlukan untuk mencapai nilai kelajuan reaksi tertentu jugalah penting. Hal ini diekspresikan oleh konstanta Michaelis-Menten (Km), yang merupakan konsentrasi substrat yang diperlukan oleh suatu enzim untuk mencapai setengah kelajuan maksimumnya. Setiap enzim memiliki nilai Km yang berbeda-beda untuk suatu subtrat, dan ini dapat menunjukkan seberapa kuatnya pengikatan substrat ke enzim. Konstanta lainnya yang juga berguna adalah kcat, yang merupakan jumlah molekul substrat yang dapat ditangani oleh satu tapak aktif per detik.
Efisiensi suatu enzim diekspresikan oleh kcat/Km. Ia juga disebut sebagai konstanta kespesifikan dan memasukkan tetapan kelajuan semua langkah reaksi. Karena konstanta kespesifikan mencermikan kemampuan katalitik dan afinitas, ia dapat digunakan untuk membandingkan enzim yang satu dengan enzim yang lain, ataupun enzim yang sama dengan substrat yang berbeda. Konstanta kespesifikan maksimum teoretis disebut limit difusi dan nilainya sekitar 108 sampai 109 (M−1 s−1). Pada titik ini, setiap penumbukkan enzim dengan substratnya akan menyebabkan katalisis, dan laju pembentukan produk tidak dibatasi oleh laju reaksi, melainkan oleh laju difusi. Enzim dengan sifat demikian disebut secara katalitik sempurna ataupun secara kinetika sempurna. Contoh enzim yang memiliki sifat seperti ini adalah karbonat anhidrase, asetilkolinesterase, katalase, fumarase, β-laktamase, dan superoksida dismutase.
Kinetika Michaelis-Menten bergantung pada hukum aksi massa, yang diturunkan berdasarkan asumsi difusi bebas dan pertumbukan acak yang didorong secara termodinamik. Namun, banyak proses-proses biokimia dan seluler yang menyimpang dari kondisi ideal ini, disebabkan oleh kesesakan makromolekuler (macromolecular crowding), perpisahan fase enzim/substrat/produk, dan pergerakan molekul secara satu atau dua dimensi.[48] Pada situasi seperti ini, kinetika Michaelis-Menten fraktal dapat diterapkan.[49][50][51][52]
Beberapa enzim beroperasi dengan kinetika yang lebih cepat daripada laju difusi. Hal ini tampaknya sangat tidak mungkin. Beberapa mekanisme telah diajukan untuk menjelaskan fenomena ini. Beberapa protein dipercayai mempercepat katalisis dengan menarik substratnya dan melakukan pra-orientasi substrat menggunakan medan listrik dipolar. Model lainnya menggunakan penjelasan penerowongan kuantum mekanika, walaupun penjelasan ini masih kontroversial.[53][54] Penerowongan kuantum untuk proton telah terpantau pada triptamina.[55]
Inhibisi
Laju reaksi enzim dapat diturunkan menggunakan berbagai jenis inhibitor enzim.
- Inhibisi kompetitif
Pada inihibisi kompetitif, inhibitor dan substrat berkompetisi untuk berikatan dengan enzim. Seringkali inhibitor kompetitif memiliki struktur yang sangat mirip dengan substrat asli enzim. Sebagai contoh, metotreksat adalah inihibitor kompetitif untuk enzim dihidrofolat reduktase. Kemiripan antara struktur asam folat dengan obat ini ditunjukkan oleh gambar di samping bawah. Perhatikan bahwa pengikatan inhibitor tidaklah perlu terjadi pada tapak pengikatan substrat apabila pengikatan inihibitor mengubah konformasi enzim, sehingga menghalangi pengikatan substrat. Pada inhibisi kompetitif, kelajuan maksimal reaksi tidak berubah, tetapi memerlukan konsentrasi substrat yang lebih tinggi untuk mencapai kelajuan maksimal tersebut, sehingga meningkatkan Km.
- Inhibisi tak kompetitif
Pada inhibisi tak kompetitif, inhibitor tidak dapat berikatan dengan enzim bebas, tetapi hanya dapat dengan komples ES. Kompleks EIS yang terbentuk kemudian menjadi tidak aktif. Jenis inhibisi ini sangat jarang, tetapi dapat terjadi pada enzim-enzim multimerik.
- Inhibisi non-kompetitif
Inhibitor non-kompetitif dapat mengikat enzim pada saat yang sama substrat berikatan dengan enzim. Baik kompleks EI dan EIS tidak aktif. Karena inhibitor tidak dapat dilawan dengan peningkatan konsentrasi substrat, Vmax reaksi berubah. Namun, karena substrat masih dapat mengikat enzim, Km tetaplah sama.
- Inhibisi campuran
Inhibisis jenis ini mirip dengan inhibisi non-kompetitif, kecuali kompleks EIS memiliki aktivitas enzimatik residual.
Pada banyak organisme, inhibitor dapat merupakan bagian dari mekanisme umpan balik. Jika enzim memproduksi terlalu banyak produk, produk tersebut dapat berperan sebagai inhibitor bagi enzim tersebut. Hal ini akan menyebabkan produksi produk melambat atau berhenti. Bentuk umpan balik ini adalah umpan balik negatif. Enzim memiliki bentuk regulasi seperti ini sering kali multimerik dan mempunyai tapak ikat alosterik. Kurva substrat/kelajuan enzim ini tidak berbentuk hiperbola melainkan berbentuk S.
Inhibitor ireversibel bereaksi dengan enzim dan membentuk aduk dengan protein. Inaktivasi ini bersifat ireversible. Inhibitor seperti ini contohnya efloritina, obat yang digunakan untuk mengobati penyakit yang disebabkan oleh protozoa African trypanosomiasis.[57] Penisilin dan Aspirin juga bekerja dengan cara yang sama. Senyawa obat ini terikat pada tapak aktif, dan enzim kemudian mengubah inhibitor menjadi bentuk aktif yang bereaksi secara ireversibel dengan satu atau lebih residu asam amino.
- Kegunaan inhibitor
Oleh karena inhibitor menghambat fungsi enzim, inhibitor sering digunakan sebagai obat. Contohnya adalah inhibitor yang digunakan sebagai obat aspirin. Aspirin menginhibisi enzim COX-1 dan COX-2 yang memproduksi pembawa pesan peradangan prostaglandin, sehingga ia dapat menekan peradangan dan rasa sakit. Namun, banyak pula inhibitor enzim lainnya yang beracun. Sebagai contohnya, sianida yang merupakan inhibitor enzim ireversibel, akan bergabung dengan tembaga dan besi pada tapak aktif enzim sitokrom c oksidase dan mengeblok pernapasan sel.[58]
Fungsi biologis
Enzim mempunyai berbagai fungsi bioligis dalam tubuh organisme hidup. Enzim berperan dalam transduksi signal dan regulasi sel, seringkali melalui enzim kinase dan fosfatase.[59] Enzim juga berperan dalam menghasilkan pergerakan tubuh, dengan miosin menghidrolisis ATP untuk menghasilkan kontraksi otot.[60] ATPase lainnya dalam membran sel umumnya adalah pompa ion yang terlibat dalam transpor aktif. Enzim juga terlibat dalam fungs-fungsi yang khas, seperti lusiferase yang menghasilkan cahaya pada kunang-kunang.[61] Virus juga mengandung enzim yang dapat menyerang sel, misalnya HIV integrase dan transkriptase balik.
Salah satu fungsi penting enzim adalah pada sistem pencernaan hewan. Enzim seperti amilase dan protease memecah molekul yang besar (seperti pati dan protein) menjadi molekul yang kecil, sehingga dapat diserap oleh usus. Molekul pati, sebagai contohnya, terlalu besar untuk diserap oleh usus, tetapi enzim akan menghidrolisis rantai pati menjadi molekul kecil seperti maltosa, yang akan dihidrolisis lebih jauh menjadi glukosa, sehingga dapat diserap. Enzim-enzim yang berbeda, mencerna zat-zat makanan yang berbeda pula. Pada hewan pemamah biak, mikroorganisme dalam perut hewan tersebut menghasilkan enzim selulase yang dapat mengurai sel dinding selulosa tanaman.[62]
Beberapa enzim dapat bekerja bersama dalam urutan tertentu, dan menghasilan lintasan metabolisme. Dalam lintasan metabolisme, satu enzim akan membawa produk enzim lainnya sebagai substrat. Setelah reaksi katalitik terjadi, produk kemudian dihantarkan ke enzim lainnya. Kadang-kadang lebih dari satu enzim dapat mengatalisasi reaksi yang sama secara bersamaan.
Enzim menentukan langkah-langkah apa saja yang terjadi dalam lintasan metabolisme ini. Tanpa enzim, metabolisme tidak akan berjalan melalui langkah yang teratur ataupun tidak akan berjalan dengan cukup cepat untuk memenuhi kebutuhan sel. Dan sebenarnya, lintasan metabolisme seperti glikolisis tidak akan dapat terjadi tanpa enzim. Glukosa, contohnya, dapat bereaksi secara langsung dengan ATP, dan menjadi terfosforliasi pada karbon-karbonnya secara acak. Tanpa keberadaan enzim, proses ini berjalan dengan sangat lambat. Namun, jika heksokinase ditambahkan, reaksi ini tetap berjalan, tetapi fosforilasi pada karbon 6 akan terjadi dengan sangat cepat, sedemikiannya produk glukosa-6-fosfat ditemukan sebagai produk utama. Oleh karena itu, jaringan lintasan metabolisme dalam tiap-tiap sel bergantung pada kumpulan enzim fungsional yang terdapat dalam sel tersebut.
Kontrol aktivitas
Terdapat lima cara utama aktivitas enzim dikontrol dalam sel.
- Produksi enzim (transkripsi dan translasi gen enzim) dapat ditingkatkan atau diturunkan bergantung pada respons sel terhadap perubahan lingkungan. Bentuk regulasi gen ini disebut induksi dan inhibisi enzim. Sebagai contohnya, bakteri dapat menjadi resisten terhadap antibiotik seperti penisilin karena enzim yang disebut beta-laktamase menginduksi hidrolisis cincin beta-laktam penisilin. Contoh lainnya adalah enzim dalam hati yang disebut sitokrom P450 oksidase yang penting dalam metabolisme obat. Induksi atau inhibisi enzim ini dapat mengakibatkan interaksi obat.
- Enzim dapat dikompartemenkan, dengan lintasan metabolisme yang berbeda-beda yang terjadi dalam kompartemen sel yang berbeda. Sebagai contoh, asam lemak disintesis oleh sekelompok enzim dalam sitosol, retikulum endoplasma, dan aparat golgi, dan digunakan oleh sekelompok enzim lainnya sebagai sumber energi dalam mitokondria melalui β-oksidasi.[63]
- Enzim dapat diregulasi oleh inhibitor dan aktivator. Contohnya, produk akhir lintasan metabolisme seringkali merupakan inhibitor enzim pertama yang terlibat dalam lintasan metabolisme, sehingga ia dapat meregulasi jumlah produk akhir lintasan metabolisme tersebut. Mekanisme regulasi seperti ini disebut umpan balik negatif karena jumlah produk akhir diatur oleh konsentrasi produk itu sendiri. Mekanisme umpan balik negatif dapat secara efektif mengatur laju sintesis zat antara metabolit tergantung pada kebutuhan sel. Hal ini membantu alokasi bahan zat dan energi secara ekonomis dan menghindari pembuatan produk akhir yang berlebihan. Kontrol aksi enzimatik membantu menjaga homeostasis organisme hidup.
- Enzim dapat diregulasi melalui modifikasi pasca-translasional. Ia dapat meliputi fosforilasi, miristoilasi, dan glikosilasi. Contohnya, sebagai respon terhadap insulin, fosforilasi banyak enzim termasuk glikogen sintase membantu mengontrol sintesis ataupun degradasi glikogen dan mengizinkan sel merespons terhadap perubahan kadar gula darah.[64] Contoh lain modifikasi pasca-translasional adalah pembelahan rantai polipeptida. Kimotripsin yang merupakan protease pencernaan diproduksi dalam keadaan tidak aktif sebagai kimotripsinogen di pankreas. Ia kemudian ditranspor ke dalam lambung di mana ia diaktivasi. Hal ini menghalangi enzim mencerna pankreas dan jaringan lainnya sebelum ia memasuki lambung. Jenis prekursor tak aktif ini dikenal sebagai zimogen.
- Beberapa enzim dapat menjadi aktif ketika berada pada lingkungan yang berbeda. Contohnya, hemaglutinin pada virus influenza menjadi aktif dikarenakan kondisi asam lingkungan. Hal ini terjadi ketika virus terbawa ke dalam sel inang dan memasuki lisosom.[65]
Keterlibatan dalam penyakit
Oleh karena kontrol aktivitas enzim yang ketat diperlukan untuk menjaga homeostasis, malafungsi (mutasi, kelebihan produksi, kekurangan produksi ataupun delesi) enzim tunggal yang penting dapat menyebabkan penyakit genetik. Pentingnya enzim ditunjukkan oleh fakta bahwa penyakit-penyakit mematikan dapat disebabkan oleh hanya mala fungsi satu enzim dari ribuan enzim yang ada dalam tubuh kita.
Salah satu contohnya adalah fenilketonuria. Mutasi asam amino tunggal pada enzim fenilalania hidroksilase yang mengatalisis langkah pertama degradasi fenilalanina mengakibatkan penumpukkan fenilalanina dan senyawa terkait. Hal ini dapat menyebabkan keterbelakangan mental jika ia tidak diobati.[66]
Contoh lainnya adalah mutasi silsilah nutfah (germline mutation) pada gen yang mengkode enzim reparasi DNA. Ia dapat menyebakan sindrom penyakit kanker keturunan seperti xeroderma pigmentosum. Kerusakan ada enzim ini dapat menyebabkan kanker karena kemampuan tubuh memperbaiki mutasi pada genom menjadi berkurang. Hal ini menyebabkan akumulasi mutasi dan mengakibatkan berkembangnya berbagai jenis kanker pada penderita.
Referensi
- ^ Smith AL (Ed); et al. (1997). Oxford dictionary of biochemistry and molecular biology. Oxford [Oxfordshire]: Oxford University Press. ISBN 0-19-854768-4.
- ^ Grisham, Charles M.; Reginald H. Garrett (1999). Biochemistry. Philadelphia: Saunders College Pub. hlm. 426–7. ISBN 0-03-022318-0.
- ^ de Réaumur, RAF (1752). "Observations sur la digestion des oiseaux". Histoire de l'academie royale des sciences. 1752: 266, 461.
- ^ Williams, H. S. (1904) A History of Science: in Five Volumes. Volume IV: Modern Development of the Chemical and Biological Sciences Harper and Brothers (New York) Accessed 4 April 2007
- ^ Dubos J. (1951). "Louis Pasteur: Free Lance of Science, Gollancz. Quoted in Manchester K. L. (1995) Louis Pasteur (1822–1895)—chance and the prepared mind". Trends Biotechnol. 13 (12): 511–5. doi:10.1016/S0167-7799(00)89014-9. PMID 8595136.
- ^ Nobel Laureate Biography of Eduard Buchner at http://nobelprize.org Accessed 4 April 2007
- ^ Text of Eduard Buchner's 1907 Nobel lecture at http://nobelprize.org Accessed 4 April 2007
- ^ 1946 Nobel prize for Chemistry laureates at http://nobelprize.org Accessed 4 April 2007
- ^ Blake CC, Koenig DF, Mair GA, North AC, Phillips DC, Sarma VR. (1965). "Structure of hen egg-white lysozyme. A three-dimensional Fourier synthesis at 2 Angstrom resolution". Nature. 22 (206): 757–61. doi:10.1038/206757a0. PMID 5891407.
- ^ Chen LH, Kenyon GL, Curtin F, Harayama S, Bembenek ME, Hajipour G, Whitman CP (1992). "4-Oxalocrotonate tautomerase, an enzyme composed of 62 amino acid residues per monomer". J. Biol. Chem. 267 (25): 17716–21. PMID 1339435.
- ^ Smith S (1994). "The animal fatty acid synthase: one gene, one polypeptide, seven enzymes". Faseb J. 8 (15): 1248–59. PMID 8001737.
- ^ Anfinsen C.B. (1973). "Principles that Govern the Folding of Protein Chains". Science. 181: 223–30. doi:10.1126/science.181.4096.223. PMID 4124164.
- ^ Dunaway-Mariano D (2008). "Enzyme function discovery". Structure. 16 (11): 1599–600. doi:10.1016/j.str.2008.10.001. PMID 19000810.
- ^ The Catalytic Site Atlas at The European Bioinformatics Institute Accessed 4 April 2007
- ^ Jaeger KE, Eggert T. (2004). "Enantioselective biocatalysis optimized by directed evolution". Curr Opin Biotechnol. 15 (4): 305–13. doi:10.1016/j.copbio.2004.06.007. PMID 15358000.
- ^ Shevelev IV, Hubscher U. (2002). "The 3' 5' exonucleases". Nat Rev Mol Cell Biol. 3 (5): 364–76. doi:10.1038/nrm804. PMID 11988770.
- ^ Tymoczko, John L.; Stryer Berg Tymoczko; Stryer, Lubert; Berg, Jeremy Mark (2002). Biochemistry. San Francisco: W.H. Freeman. ISBN 0-7167-4955-6.
- ^ Zenkin N, Yuzenkova Y, Severinov K. (2006). "Transcript-assisted transcriptional proofreading". Science. 313: 518–20. doi:10.1126/science.1127422. PMID 16873663.
- ^ Ibba M, Soll D. (2000). "Aminoacyl-tRNA synthesis". Annu Rev Biochem. 69: 617–50. doi:10.1146/annurev.biochem.69.1.617. PMID 10966471.
- ^ Rodnina MV, Wintermeyer W. (2001). "Fidelity of aminoacyl-tRNA selection on the ribosome: kinetic and structural mechanisms". Annu Rev Biochem. 70: 415–35. doi:10.1146/annurev.biochem.70.1.415. PMID 11395413.
- ^ Firn, Richard. "The Screening Hypothesis - a new explanation of secondary product diversity and function". Diakses tanggal 2006-10-11.
- ^ Fischer E. (1894). "Einfluss der Configuration auf die Wirkung der Enzyme". Ber. Dt. Chem. Ges. 27: 2985–93. doi:10.1002/cber.18940270364. line feed character di
|journal=pada posisi 9 (bantuan) - ^ Koshland D. E. (1958). "Application of a Theory of Enzyme Specificity to Protein Synthesis". Proc. Natl. Acad. Sci. 44 (2): 98–104. doi:10.1073/pnas.44.2.98. PMID 16590179.
- ^ Vasella A, Davies GJ, Bohm M. (2002). "Glycosidase mechanisms". Curr Opin Chem Biol. 6 (5): 619–29. doi:10.1016/S1367-5931(02)00380-0. PMID 12413546.
- ^ Boyer, Rodney (2002) [2002]. "6". Concepts in Biochemistry (edisi ke-2nd). New York, Chichester, Weinheim, Brisbane, Singapore, Toronto.: John Wiley & Sons, Inc. hlm. 137–8. ISBN 0-470-00379-0. OCLC 51720783.
- ^ Fersht, Alan (1985). Enzyme structure and mechanism. San Francisco: W.H. Freeman. hlm. 50–2. ISBN 0-7167-1615-1.
- ^ Jencks, William P. (1987). Catalysis in chemistry and enzymology. Mineola, N.Y: Dover. ISBN 0-486-65460-5.
- ^ Villa J, Strajbl M, Glennon TM, Sham YY, Chu ZT, Warshel A (2000). "How important are entropic contributions to enzyme catalysis?". Proc. Natl. Acad. Sci. U.S.A. 97 (22): 11899–904. doi:10.1073/pnas.97.22.11899. PMID 11050223.
- ^ Warshel A, Sharma PK, Kato M, Xiang Y, Liu H, Olsson MH (2006). "Electrostatic basis for enzyme catalysis". Chem. Rev. 106 (8): 3210–35. doi:10.1021/cr0503106. PMID 16895325.
- ^ Eisenmesser EZ, Bosco DA, Akke M, Kern D (2002). "Enzyme dynamics during catalysis". Science. 295 (5559): 1520–3. doi:10.1126/science.1066176. PMID 11859194.
- ^ Agarwal PK (2005). "Role of protein dynamics in reaction rate enhancement by enzymes". J. Am. Chem. Soc. 127 (43): 15248–56. doi:10.1021/ja055251s. PMID 16248667.
- ^ Eisenmesser EZ, Millet O, Labeikovsky W; et al. (2005). "Intrinsic dynamics of an enzyme underlies catalysis". Nature. 438 (7064): 117–21. doi:10.1038/nature04105. PMID 16267559.
- ^ Yang LW, Bahar I (5 June 2005). "Coupling between catalytic site and collective dynamics: A requirement for mechanochemical activity of enzymes". Structure. 13: 893–904. doi:10.1016/j.str.2005.03.015. PMID 15939021.
- ^ Agarwal PK, Billeter SR, Rajagopalan PT, Benkovic SJ, Hammes-Schiffer S. (5 March 2002). "Network of coupled promoting motions in enzyme catalysis". Proc Natl Acad Sci USA. 99: 2794–9. doi:10.1073/pnas.052005999. PMID 11867722.
- ^ Agarwal PK, Geist A, Gorin A (2004). "Protein dynamics and enzymatic catalysis: investigating the peptidyl-prolyl cis-trans isomerization activity of cyclophilin A". Biochemistry. 43 (33): 10605–18. doi:10.1021/bi0495228. PMID 15311922.
- ^ Tousignant A, Pelletier JN. (2004). "Protein motions promote catalysis". Chem Biol. 11 (8): 1037–42. doi:10.1016/j.chembiol.2004.06.007. PMID 15324804.
- ^ Olsson MHM, Parson WW, Warshel A (2006). "Dynamical Contributions to Enzyme Catalysis: Critical Tests of A Popular Hypothesis". Chem. Rev. 106 (5): 1737–56. doi:10.1021/cr040427e.
- ^ a b de Bolster, M.W.G. (1997). "Glossary of Terms Used in Bioinorganic Chemistry: Cofactor". International Union of Pure and Applied Chemistry. Diakses tanggal 2007-10-30.
- ^ Fisher Z, Hernandez Prada JA, Tu C, Duda D, Yoshioka C, An H, Govindasamy L, Silverman DN and McKenna R. (2005). "Structural and kinetic characterization of active-site histidine as a proton shuttle in catalysis by human carbonic anhydrase II". Biochemistry. 44 (4): 1097–115. doi:10.1021/bi0480279. PMID 15667203.
- ^ Wagner, Arthur L. (1975). Vitamins and Coenzymes. Krieger Pub Co. ISBN 0-88275-258-8.
- ^ de Bolster, M.W.G. (1997). "Glossary of Terms Used in Bioinorganic Chemistry: Coenzyme". International Union of Pure and Applied Chemistry. Diakses tanggal 2007-10-30.
- ^ BRENDA The Comprehensive Enzyme Information System Accessed 4 April 2007
- ^ Henri, V. (1902). "Theorie generale de l'action de quelques diastases". Compt. Rend. Hebd. Acad. Sci. Paris. 135: 916–9.
- ^ Sørensen,P.L. (1909). "Enzymstudien {II}. Über die Messung und Bedeutung der Wasserstoffionenkonzentration bei enzymatischen Prozessen". Biochem. Z. 21: 131–304.
- ^ Michaelis L., Menten M. (1913). "Die Kinetik der Invertinwirkung". Biochem. Z. 49: 333–369. English translation Accessed 6 April 2007
- ^ Briggs G. E., Haldane J. B. S. (1925). "A note on the kinetics of enzyme action". Biochem. J. 19: 339–339. PMID 16743508.
- ^ Radzicka A, Wolfenden R. (1995). "A proficient enzyme". Science. 6 (267): 90–931. doi:10.1126/science.7809611. PMID 7809611.
- ^ Ellis RJ (2001). "Macromolecular crowding: obvious but underappreciated". Trends Biochem. Sci. 26 (10): 597–604. doi:10.1016/S0968-0004(01)01938-7. PMID 11590012.
- ^ Kopelman R (1988). "Fractal Reaction Kinetics". Science. 241 (4873): 1620–26. doi:10.1126/science.241.4873.1620. PMID 17820893.
- ^ Savageau MA (1995). "Michaelis-Menten mechanism reconsidered: implications of fractal kinetics". J. Theor. Biol. 176 (1): 115–24. doi:10.1006/jtbi.1995.0181. PMID 7475096.
- ^ Schnell S, Turner TE (2004). "Reaction kinetics in intracellular environments with macromolecular crowding: simulations and rate laws". Prog. Biophys. Mol. Biol. 85 (2–3): 235–60. doi:10.1016/j.pbiomolbio.2004.01.012. PMID 15142746.
- ^ Xu F, Ding H (2007). "A new kinetic model for heterogeneous (or spatially confined) enzymatic catalysis: Contributions from the fractal and jamming (overcrowding) effects". Appl. Catal. A: Gen. 317 (1): 70–81. doi:10.1016/j.apcata.2006.10.014.
- ^ Garcia-Viloca M., Gao J., Karplus M., Truhlar D. G. (2004). "How enzymes work: analysis by modern rate theory and computer simulations". Science. 303 (5655): 186–95. doi:10.1126/science.1088172. PMID 14716003.
- ^ Olsson M. H., Siegbahn P. E., Warshel A. (2004). "Simulations of the large kinetic isotope effect and the temperature dependence of the hydrogen atom transfer in lipoxygenase". J. Am. Chem. Soc. 126 (9): 2820–8. doi:10.1021/ja037233l. PMID 14995199.
- ^ Masgrau L., Roujeinikova A., Johannissen L. O., Hothi P., Basran J., Ranaghan K. E., Mulholland A. J., Sutcliffe M. J., Scrutton N. S., Leys D. (2006). "Atomic Description of an Enzyme Reaction Dominated by Proton Tunneling". Science. 312 (5771): 237–41. doi:10.1126/science.1126002. PMID 16614214.
- ^ Cleland, W.W. (1963). "The Kinetics of Enzyme-catalyzed Reactions with two or more Substrates or Products 2. {I}nhibition: Nomenclature and Theory". Biochim. Biophys. Acta. 67: 173–87.
- ^ Poulin R, Lu L, Ackermann B, Bey P, Pegg AE. Mechanism of the irreversible inactivation of mouse ornithine decarboxylase by alpha-difluoromethylornithine. Characterization of sequences at the inhibitor and coenzyme binding sites. J Biol Chem. 1992 January 5;267(1):150–8. PMID 1730582
- ^ Yoshikawa S and Caughey WS. (1990). "Infrared evidence of cyanide binding to iron and copper sites in bovine heart cytochrome c oxidase. Implications regarding oxygen reduction". J Biol Chem. 265 (14): 7945–58. PMID 2159465.
- ^ Hunter T. (1995). "Protein kinases and phosphatases: the yin and yang of protein phosphorylation and signaling". Cell. 80 (2): 225–36. doi:10.1016/0092-8674(95)90405-0. PMID 7834742.
- ^ Berg JS, Powell BC, Cheney RE (2001). "A millennial myosin census". Mol. Biol. Cell. 12 (4): 780–94. PMC 32266 . PMID 11294886.
- ^ Meighen EA (1991). "Molecular biology of bacterial bioluminescence". Microbiol. Rev. 55 (1): 123–42. PMC 372803 . PMID 2030669.
- ^ Mackie RI, White BA (1990). "Recent advances in rumen microbial ecology and metabolism: potential impact on nutrient output". J. Dairy Sci. 73 (10): 2971–95. PMID 2178174.
- ^ Faergeman NJ, Knudsen J (1997). "Role of long-chain fatty acyl-CoA esters in the regulation of metabolism and in cell signalling". Biochem. J. 323 (Pt 1): 1–12. PMC 1218279 . PMID 9173866.
- ^ Doble B. W., Woodgett J. R. (2003). "GSK-3: tricks of the trade for a multi-tasking kinase". J. Cell. Sci. 116: 1175–86. doi:10.1242/jcs.00384. PMID 12615961.
- ^ Carr C. M., Kim P. S. (2003). "A spring-loaded mechanism for the conformational change of influenza hemagglutinin". Cell. 73: 823–32. doi:10.1016/0092-8674(93)90260-W. PMID 8500173.
- ^ Phenylketonuria: NCBI Genes and Disease Accessed 4 April 2007